题目内容
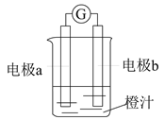
【题目】课堂学习中,同学们利用镁条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组成。下列结论正确的是
A. 原电池是将电能转化成化学能的装置
B. 实验探究中,活泼性强的金属做正极,活泼性弱的金属做负极
C. 上图中a极为锌片、b极为镁条时,导线中会产生电流
D. 上图中a极为锌片、b极为铜片时,电子由铜片通过导线流向锌片
【答案】C
【解析】
A.原电池是将化学能转变为电能的装置,故A错误;
B.原电池由两个电极、电解质溶液和导线等组成,橙汁显酸性,活泼性强的金属做负极,活泼性弱的金属做正极,故B错误;
C.图中a极为锌片、b极为镁条时,镁和橙汁能自发的进行氧化还原反应,所以能构成原电池,则导线中会产生电流,故C正确;
D.图中a极为锌片、b极为铜片时,锌易失电子而作负极,铜作正极,原电池放电时,电子由负极锌片通过导线流向铜片,故D错误;
故选C。

练习册系列答案
相关题目