题目内容
【题目】下列指定反应的离子方程式正确的是( )
A.用饱和Na2CO3溶液浸泡CaSO4固体:CO![]() +CaSO4
+CaSO4![]() CaCO3+SO
CaCO3+SO![]()
B.向NH4HCO3溶液中加入足量石灰水:Ca2++HCO![]() +OH-=CaCO3↓+H2O
+OH-=CaCO3↓+H2O
C.向CuSO4溶液中加过量的氨水:Cu2++2NH3·H2O=Cu(OH)2↓+2NH![]()
D.用碘化钾淀粉溶液检验亚硝酸钠中NO![]() 的存在:NO
的存在:NO![]() +2I-+2H+=NO↑+I2+H2O
+2I-+2H+=NO↑+I2+H2O
【答案】A
【解析】
A.碳酸钙溶解度小于硫酸钙,锅炉水垢中的CaSO4用饱和Na3CO3溶液浸泡后可以转化为碳酸钙,离子方程式:CO![]() +CaSO4
+CaSO4![]() CaCO3+SO
CaCO3+SO![]() ,故A正确;
,故A正确;
B.向碳酸氢铵溶液中加入足量石灰水,铵根离子和碳酸氢根离子都参与反应,正确的离子方程式为:NH4++HCO3-+Ca2++2OH-═CaCO3↓+H2O+NH3H2O,故B错误;
C.硫酸铜溶液中加过量氨水,生成络合物,离子反应为Cu2++4NH3H2O═[Cu(NH3)4]2++4H2O,故C错误;
D.用碘化钾淀粉溶液检验亚硝酸钠中NO2-的存在的离子反应为2NO2-+2I-+4H+═2NO↑+I2+2H2O,原离子方程式电荷不守恒,故D错误。
答案选A。

【题目】在800℃时,2L密闭容器内发生反应:2NO(g)+O2(g)2NO2(g),反应体系中,一氧化氮的物质的量随时间的变化如表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)如图表示NO2的物质的量浓度变化的曲线是________。
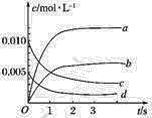
(2)用O2表示从0~2 s内该反应的平均速率v=__________。
(3)能说明该反应已达到平衡状态的是________。
A.v(NO2)=2v(O2)
B.容器内压强保持不变
C.容器内气体质量不变
D.容器内密度保持不变
【题目】某科研小组采用电解锰粉(主要成分为Mn和少量含Fe、Ni、Pb、P、Si等元素的单质或其化合物)为原料制备高纯氯化锰。
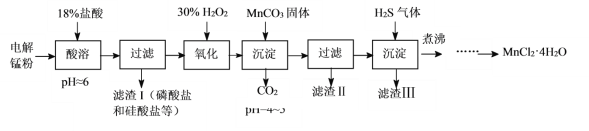
已知:①Mn是一种比Fe活泼的金属。
②H2S气体具有较强的还原性,如:H2S+H2O2=S↓+2H2O。
③相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)
Fe3+ | Fe2+ | Mn2+ | Ni2+ | Pb2+ | |
开始沉淀的pH | 1.1 | 5.8 | 8.6 | 6.7 | 8.0 |
沉淀完全的pH | 3.2 | 8.8 | 10.1 | 9.2 | 8.8 |
(1)酸溶时盐酸要缓慢滴加的原因是___。
(2)加入MnCO3固体时发生反应的离子方程式为___。MnCO3固体也可用下列物质代替___。(填写编号)
A.MnO B.MnSO4 C.Mn(OH)2 D.MnCl2
(3)通入H2S气体可使Pb2+、Ni2+生成硫化物沉淀,如:H2S(aq)+Pb2+(aq)![]() PbS(s)+2H+(aq),该反应的平衡常数K=___[用Ka1(H2S)、Ka2(H2S)及Ksp(PbS)表示]。
PbS(s)+2H+(aq),该反应的平衡常数K=___[用Ka1(H2S)、Ka2(H2S)及Ksp(PbS)表示]。
(4)煮沸的目的是___。
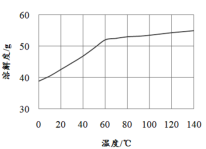
(5)已知MnCl2·4H2O在106℃时失去一分子结晶水,198℃失去全部结晶水。请补充完整由煮沸后的滤液获得高纯(>99.99%)MnCl2·4H2O晶体(MnCl2的溶解度曲线如图所示)的实验方案:将煮沸后的滤液冷却至室温,___(实验中须使用的试剂是:30%H2O2)。