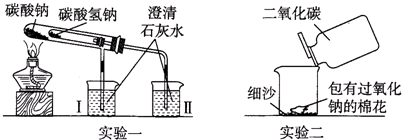
题目内容
科学家用NaNO3和Na2O在一定条件下化合制得由钠离子和阴离子B构成晶体NaxNO4,测定阴离子B中的各原子的最外层电子都达到了8电子稳定结构。下列说法错误的是
( )
( )
| A.x="3"
| B.N的化合价为+3 |
| C.阴离子B电子式可能为 | |
| D.此反应是非氧化还原反应 |
B
NaNO3+ (x-1)/2Na2O= NaxNO4,有O守恒则x=3;每个氮原子的价电子数为5,
每个氧原子的价电子数为6,1个NO43-离子中,含有1个氮原子和4个氧原子,并带3个
单位的负电荷,每个NO43-的电子总数为1×5+4×6+3=32,32可以写成4×8,根据题意可
知,Na3NO4中各原子最外层电子数都达到了8电子稳定结构,所以NO43-的
电子式为: ,氮的化合价为+5。
,氮的化合价为+5。
每个氧原子的价电子数为6,1个NO43-离子中,含有1个氮原子和4个氧原子,并带3个
单位的负电荷,每个NO43-的电子总数为1×5+4×6+3=32,32可以写成4×8,根据题意可
知,Na3NO4中各原子最外层电子数都达到了8电子稳定结构,所以NO43-的
电子式为:
 ,氮的化合价为+5。
,氮的化合价为+5。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
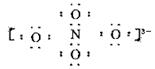
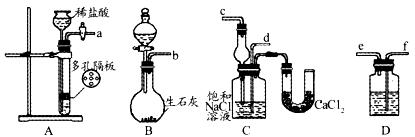

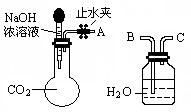
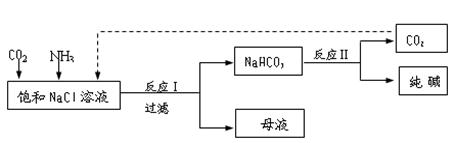
 NaHCO3↓+NH4Cl,处理母液的两种方法如下。
NaHCO3↓+NH4Cl,处理母液的两种方法如下。