题目内容
【题目】“活化分子”是衡量化学反应速率快慢的重要依据,下列对“活化分子”的说法中不正确的是( )
A.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加
B.增大反应物的浓度,可使单位体积内活化分子增多,反应速率加快
C.对于有气体参加的反应通过压缩容器增大压强,可使单位体积内活化分子增多,反应速率加快
D.活化分子之间的碰撞一定是有效碰撞
【答案】D
【解析】升高温度、加入催化剂能提高活化分子百分数;增加反应物浓度,增大体系压强只增大单位体积活化分子的数目,百分数不变;能发生化学反应的碰撞是有效碰撞,活化分子之间的碰撞不一定能发生反应,所以不一定是有效碰撞;故D错误;所以选D.

练习册系列答案
相关题目
【题目】下列实验现象所对应的离子方程式不正确的是( )
实 验 | 现 象 | 离子方程式 | |
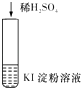
A |
| 在空气中放置一段时间后,溶液呈蓝色 | 4H++4I﹣+O2═2I2+2H2O |
B |
| 溶液由浅绿色变为红色 | 2Fe2++Cl2═2Fe3++2Cl﹣、 |
C |
| 溶液由黄绿色变为无色 | Cl2+2OH﹣═Cl﹣+ClO﹣+H2O |
D |
| 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH﹣+H++SO |
A.A
B.B
C.C
D.D
【题目】将X气体通入Y溶液中,实验结果与预测的现象一致的组合是( )
X气体 | Y溶液 | 预测的现象 |
| |
① | CO2 | 饱和Na2CO3溶液 | 白色沉淀析出 | |
② | SO2 | Ba(NO3)2溶液 | 白色沉淀析出 | |
③ | Cl2 | AgNO3溶液 | 白色沉淀析出 | |
④ | NH3 | AlCl3溶液 | 白色沉淀析出 |
A.只有①②③
B.只有①②④
C.只有①③④
D.①②③④