题目内容
12.在干燥烧瓶中用向下排空气法收集氨气,由于空气不可能排净,所以瓶内气体对氢气的相对密度为9.5,则:(1)该干燥烧瓶中混合气体的平均摩尔质量为多少?(2)氨气与空气的体积比为多少?
分析 (1)瓶内气体对氢气的相对密度为9.5,结合$\frac{M混}{M({H}_{2})}$=9.5计算;
(2)设氨气与空气的体积分别为x、y,体积之比等于物质的量比,结合M混=$\frac{17x+29y}{x+y}$计算.
解答 解:(1)瓶内气体对氢气的相对密度为9.5,由$\frac{M混}{M({H}_{2})}$=9.5可知,该干燥烧瓶中混合气体的平均摩尔质量为2g/mol×9.5=19g/mol,
答:该干燥烧瓶中混合气体的平均摩尔质量为19g/mol;
(2)设氨气与空气的体积分别为x、y,体积之比等于物质的量比,
则$\frac{17x+29y}{x+y}$=19,解得x:y=5:1,
答:氨气与空气的体积比为5:1.
点评 本题考查物质的量的计算,为高频考点,把握物质的量、平均摩尔质量的关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
3.下列操作方法不正确的是( )
| A. | 用酒精清洗沾在皮肤上的少量苯酚 | B. | 用灼烧的方法检验羊毛线和棉线 | ||
| C. | 银镜反应后的试管用稀硝酸清洗 | D. | 用分液漏斗分离苯和甲苯 |
7.在一定温度下,可逆反应A2(g)+B2(g)?2AB(g)达到平衡的标志是( )
| A. | A2、B2、AB的浓度相等 | |
| B. | 容器中的压强不再随时间变化而变化 | |
| C. | A2、B2、AB的浓度之比为1:1:2 | |
| D. | 单位时间内生成n mol A2的同时生成2n molAB |
4.对于药品的使用和作用下列说法不正确的是( )
| A. | 青霉素对病原体有抑制和杀灭作用,但在使用之前要进行过敏性实验 | |
| B. | 吗啡、海洛因等虽有麻醉、止痛、镇静作用,但易上瘾且有害,这类物质属于毒品 | |
| C. | 青霉素是一种天然抗生素 | |
| D. | R表示非处方药,OTC表示处方药 |
1.质量分数为a%的NaOH溶液蒸发掉b g水后,得到V mL质量分数为2a%的NaOH溶液,则蒸发后NaOH溶液的物质的量浓度为( )
| A. | $\frac{ab}{2V}$mol.L-1 | B. | $\frac{ab}{2000V}$mol.L-1 | C. | $\frac{250ab}{V}$mol.L-1 | D. | $\frac{ab}{80V}$mol.L-1 |
2.用NA表示阿伏德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2L氦气中原子数为NA | |
| B. | 常温常压下,1.06gNa2CO3中阴离子电荷数为0.02NA | |
| C. | 标准状况下,22.4LCCl4中的分子个数为NA | |
| D. | 0.5mol/L的MgCl2溶液中的氯离子个数为NA |
 甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色.
甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色.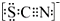 .甲同学猜想SCN-可能被Cl2氧化了,他进行了如下研究.
.甲同学猜想SCN-可能被Cl2氧化了,他进行了如下研究. 羟胺(NH2OH)是一种不稳定的白色大片状或针状结晶.极易吸潮,极易溶于水,在热水中易分解.回答下列问题:
羟胺(NH2OH)是一种不稳定的白色大片状或针状结晶.极易吸潮,极易溶于水,在热水中易分解.回答下列问题: .
.