题目内容
【题目】1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式为( )
A. C+H2O==CO+H2ΔH==+131.3KJ·mol—1
B. C(s)+H2O(g)==CO(g)+H2(g)ΔH==+10.94KJ·mol—1
C. C(s)+H2O(l)==CO(g)+H2(g)ΔH==+131.3KJ·mol—1
D. C(s)+H2O(g)==CO(g)+H2(g)ΔH==+131.3KJ·mol—1
【答案】D
【解析】试题分析:由1g碳与适量水蒸气反应生成CO和H2,需吸收10.94kJ热量,则1mol碳与水蒸气反应,吸收10.94KJ×12=131.28kJ,则此反应的热化学方程式为C(s)+H2O(g)═CO(g)+H2(g)△H=+131.28kJmol﹣1

练习册系列答案
相关题目
用图中所示的装置进行实验,实验现象与预测不一致的是( )

选项 | ①中的物质 | ②中的物质 | 预测现象 |
A | 浓氨水 | FeCl3溶液 | ②中有红褐色沉淀 |
B | 浓氨水 | 浓盐酸 | ③中有白烟 |
C | 浓硝酸 | 淀粉KI溶液 | ②中溶液无明显变化 |
D | 浓盐酸 | 酚酞溶液 | ②中溶液无明显变化 |
A. A B. B C. C D. D
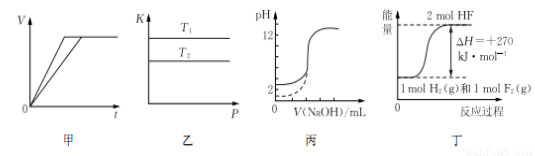
 2SO3(g) (ΔH<0)的平衡常数K与压强P的关系,且T1<T2
2SO3(g) (ΔH<0)的平衡常数K与压强P的关系,且T1<T2