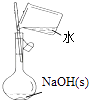题目内容
【题目】请回答:
(1)H2O2的电子式 .
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由 .
(3)完成以下氧化还原反应的离子方程式:MnO﹣4+C2O2﹣4+=Mn2++CO2↑+ .
【答案】
(1)![]()
(2)2Mg+CO2 ![]() 2MgO+C
2MgO+C
(3)2;5;16H+;16H+;10;8H2O
【解析】解:(1)双氧水为共价化合物,分子中存在两个氧氢键和一个O﹣O键,双氧水的电子式为 ![]() ,所以答案是:
,所以答案是: ![]() ;(2)镁与二氧化碳反应生成碳与氧化镁,化学方程式:2Mg+CO2
;(2)镁与二氧化碳反应生成碳与氧化镁,化学方程式:2Mg+CO2 ![]() 2MgO+C,碳能够燃烧,所以镁燃烧不能用CO2灭火;所以答案是:2Mg+CO2
2MgO+C,碳能够燃烧,所以镁燃烧不能用CO2灭火;所以答案是:2Mg+CO2 ![]() 2MgO+C;(3)Mn元素的化合价由+7价降低为+2价,C元素的化合价由+3价升高为+4价,要想使氧化剂得到电子数等于还原剂失去电子数,则高锰酸根离子系数为2,草酸根离子系数为5,依据原子个数守恒,反应的方程式:2MnO4﹣+5C2O42﹣+16H+═2Mn2++10CO2↑+8H2O;所以答案是:2;5;16H+;2;10;8H2O;
2MgO+C;(3)Mn元素的化合价由+7价降低为+2价,C元素的化合价由+3价升高为+4价,要想使氧化剂得到电子数等于还原剂失去电子数,则高锰酸根离子系数为2,草酸根离子系数为5,依据原子个数守恒,反应的方程式:2MnO4﹣+5C2O42﹣+16H+═2Mn2++10CO2↑+8H2O;所以答案是:2;5;16H+;2;10;8H2O;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
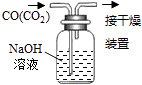
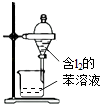
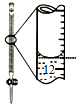
【题目】下列有关实验的选项正确的是( )
A.配制0.10molL﹣1NaOH溶液 | B.除去CO中的CO2 | C.苯萃取碘水中I2 , 分出水层后的操作 | D.记录滴定终点读数为12.20mL |
|
|
|
|
A.A
B.B
C.C
D.D