题目内容
某温度下,在(1)若x=0,y=0,则z=___________。
(2)若x=0.75,则y=___________,z=___________。
(3)x、y、z应该满足的一般条件是(用两个联立方程式表示)___________或___________。
解析:在温度、容器容积不变达到平衡时,平衡混和气体各组分的含量保持不变,这只有一种情况,即把各初始加入量转化为生成物为0或反应物为0的量来进行比较,所得到的量必须相同。
(1)x=0,y=0即把题给的x=1,y=3,转化为z=2。
(2)x=0.75,即N2转化了0.25,则H2转化了0.75,故y=2.25,生成NH3 0.5,即z=0.5。
(3)根据: N2+3H2![]() 2NH3
2NH3
起始1 1 3 0
变化 1-x 3-y z
起始2 x y z
则有![]() ,得y=3x,
,得y=3x,
![]() ,得
,得![]() ,
,
![]() ,得
,得![]() ,
,
则方程组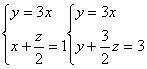
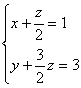
![]()
答案:(1)z=2 (2)y=2.25 z=0.5
(3)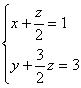 或
或![]()

| |||||||||||||||
合成氯是人类研究的重要课题,目前工业合成氨的原理为:
N2(g)+3H2(g)  2NH3(g) ΔH=-93.0kJ/mol
2NH3(g) ΔH=-93.0kJ/mol
(1)某温度下,在2 L密闭容器中发生上述反应,测得数据如下
??????????? 时间/h 物质的量/mol | 0 | 1 | 2 | 3 | 4 |
N2 | 2.0 | 1.83 | 1.7 | 1.6 | 1.6 |
H2 | 6.0 | 5.49 | 5.1 | 4.8 | 4.8 |
NH3 | 0 | 0.34 | 0.6 | 0.8 | 0.8 |
①0~2 h内,v(N2)=??????????? 。
②平衡时,H2的转化率为____;该温度下,反应2NH3(g)  N2(g)+3H2(g)的平衡常数K=?? 。
N2(g)+3H2(g)的平衡常数K=?? 。
③若保持温度和体积不变,起始投入的N2、H2、NH3的物质的量分别为a mol、b mol、c mol,达到平衡后,NH3比的浓度与上表中相同的为?????? (填选项字母)。
A.a=l、b=3.c=0? ?????? B.a=4、b=12、c=0
C.a=0、b=0.c=4? ???? D.a=l、b=3、c=2
(2)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热ΔH=-286kJ/mol,则陪制NH3反应的热化学方程式为 ??????? 。
(3)采用高质子导电性的SCY陶瓷(能传递H'),通过电解法也可合成氨,原理为:
N2(g)+3H2(g)  2NH3(g)。在电解法合成氨的过程申,应将N2不断地通入?? ___极,该电极反应式为?????????????????????? 。
2NH3(g)。在电解法合成氨的过程申,应将N2不断地通入?? ___极,该电极反应式为?????????????????????? 。