题目内容
(9分)某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物NH3性质的探究。
(1)实验室制取氨气的化学方程式为 。
(2)某同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的? (填“能”或“否”),理由是 。
(3)该小组的同学设计了如图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性。
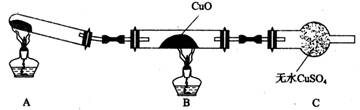
①该装置在设计上有一定缺陷。为保证实验结果的准确性,对该装置的改进措施是
。
②利用改进后的装置进行实验,CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。氨气与CuO反应的化学方程式为 。
③有同学认为NH3与CuO反应生成的红色物质中可能含Cu2O。Cu2O在酸性溶液中Cu+歧化生成Cu和Cu2+。请设计一个简单的实验检验该红色物质中是否含有Cu2O
。
(1)2NH4Cl+Ca(OH)2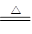 CaCl2+2NH3↑+2H2O(2分)
CaCl2+2NH3↑+2H2O(2分)
(2)否(1分) 氨气极易溶于水、氯化铵对氨气在水中的溶解影响不大(1分)
(3)①在装置A与B之间增加装有碱石灰的干燥管(1分)
②3CuO+2NH3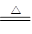 3Cu+N2+3H2O(2分)
3Cu+N2+3H2O(2分)
③取少许样品,加入稀H2SO4,若溶液出现蓝色,说明含有Cu2O,反之则没有(2分)
【解析】
试题分析:(1)实验室制取氨气的化学方程式为2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
(2)由于氨气极易溶于水、氯化铵对氨气在水中的溶解影响不大,所以不能用排饱和氯化铵溶液的方法收集氨气。
(3)①由于生成的氨气中含有水蒸气,从而干扰实验的验证,所以需要在装置A与B之间增加装有碱石灰的干燥管来干燥氨气。
②根据原子守恒可知,没有污染的气体应该是氮气,所以反应的化学方程式是3CuO+2NH3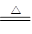 3Cu+N2+3H2O。
3Cu+N2+3H2O。
③根据题意可知,Cu2O在酸性溶液中Cu+歧化生成Cu和Cu2+而使溶液显蓝色,据此可以验证,但该酸不能是氧化性酸,所以可以用盐酸或稀硫酸。因此正确的操作是:取少许样品,加入稀H2SO4,若溶液出现蓝色,说明含有Cu2O,反之则没有。
考点:考查氨气的制备、性质以及物质的检验等
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。

(5分)某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:
| 实验编号 | 水果种类 | 电极间距离/㎝ | 电流大小/µA |
| ① | 西红柿 | 1 | 98.7 |
| ② | 西红柿 | 2 | 72.5 |
| ③ | 苹 果 | 2 | 27.2 |
(2)上图所示的装置中,做负极的材料是_______(填“铜片”或“锌片”),该装置能将______转变为电能。
(3)能表明水果种类对电流大小有影响的实验编号是________和__________。
(4)请你再提出一个可能影响水果电池电流大小的因素:__________________________。
(5分)某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:

|
实验编号 |
水果种类 |
电极间距离/㎝ |
电流大小/µA |
|
① |
西红柿 |
1 |
98.7 |
|
② |
西红柿 |
2 |
72.5 |
|
③ |
苹 果 |
2 |
27.2 |
(1)该实验的目的是探究水果种类和_______________对水果电池电流大小的影响。
(2)上图所示的装置中,做负极的材料是_______(填“铜片”或“锌片”),该装置能将______转变为电能。
(3)能表明水果种类对电流大小有影响的实验编号是________和__________。
(4)请你再提出一个可能影响水果电池电流大小的因素:__________________________。
 (08云南昆明质量检测,9)某校研究性学习小组利用铁生锈原理设计了一个可给收音机供电的装置。在此装置中,下列说法正确的是( )
(08云南昆明质量检测,9)某校研究性学习小组利用铁生锈原理设计了一个可给收音机供电的装置。在此装置中,下列说法正确的是( )