题目内容
(4分)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,请回答下列问题:
(1)反应开始到10s,用X表示的反应速率为
(2)反应的化学方程式为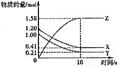
(1)反应开始到10s,用X表示的反应速率为
(2)反应的化学方程式为

ν(X)=ν(Y)=0.0395mol/(L·s) X(g)+Y(g)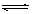 2Z(g)
2Z(g)
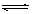 2Z(g)
2Z(g)略

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
题目内容

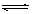 2Z(g)
2Z(g)
 口算能手系列答案
口算能手系列答案