题目内容
实验室中用浓盐酸与MnO2制Cl2,再用Cl2和Ca(OH)2制少量漂白粉。已知Cl2和Ca(OH)2反应制漂白粉的反应是放热反应,温度稍高即发生副反应:6Cl2+6Ca(OH)2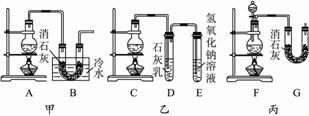
解析:本题的综合性较强,既需要熟悉Cl2的制法,又要抓住题给的信息,应用理论知识采取相应的措施。根据题给试剂、信息和Cl2的毒性,对以上三套装置进行分析和评价,注意每一套装置的优缺点。
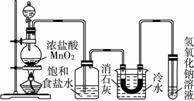
答案:首先三套装置都缺少Cl2的净化装置(Cl2中含有HCl)。除此之外,甲的设计中气体的发生无法控制,且没有尾气吸收装置,会污染环境;乙的设计中气体的发生也无法控制,且没有降温装置,会导致副反应发生;丙的设计也没有降温装置和尾气吸收装置。但他们的设计都有合理的部分,如丙的气体发生装置F,甲的反应降温装置B,乙的尾气吸收装置E等。把它们进行组合,便可以组成一套更加完善的实验装置(如下图所示)。

 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案(10分)实验室中用浓盐酸与MnO2制取Cl2,再用Cl2和Ca(OH)2反应制少量漂白粉。已知Cl2和Ca(OH)2制漂白粉是放热反应,温度稍高易发生副反应:
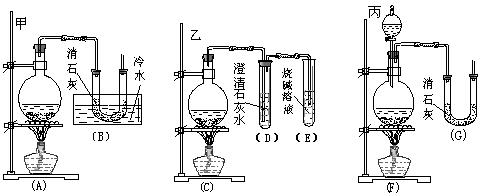
6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。现有三位同学分别设计的三套实验装置如下(U形管中放有玻璃纤维,气体能顺利通过):
(1)请从以下六方面对上述甲、乙、丙三套装置的优缺点进行评价,将适当的选项序号填于下表内:
a.不易控制反应速率 b.容易控制反应速率 c.有副反应发生
d.可防止副反应发生 e.容易污染环境 f.可防止污染环境
|
| 优点 | 缺点 |
| 甲装置 |
|
|
| 乙装置 |
|
|
| 丙装置 |
|
|
(2)请从甲、乙、丙三套装置中,选取合理的组成部分(A、B、C、D、E、F、G),组装一套你认为更完善的实验装置,连接顺序(按气流从左到右的方向)为 ;在此装置及甲、乙、丙三装置中,你认为是否还缺少必要的装置,并说明原因
。
(3)如果反应前加入了m g Ca(OH)2,反应结束并冷却后倒出固体物质称量为n g(设反应中产生的水仍留在固体物质中)。则该固体物质中Ca(ClO)2的质量分数的表达式为(不必化简): 。
(10分)实验室中用浓盐酸与MnO2制取Cl2,再用Cl2和Ca(OH)2反应制少量漂白粉。已知Cl2和Ca(OH)2制漂白粉是放热反应,温度稍高易发生副反应:
6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。现有三位同学分别设计的三套实验装置如下(U形管中放有玻璃纤维,气体能顺利通过):
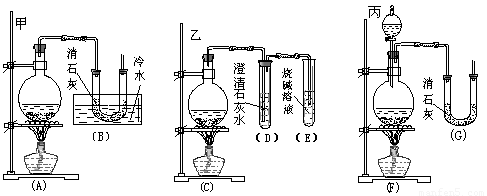
(1)请从以下六方面对上述甲、乙、丙三套装置的优缺点进行评价,将适当的选项序号填于下表内:
a.不易控制反应速率 b.容易控制反应速率 c.有副反应发生
d.可防止副反应发生 e.容易污染环境 f.可防止污染环境
|
|
优点 |
缺点 |
|
甲装置 |
|
|
|
乙装置 |
|
|
|
丙装置 |
|
|
(2)请从甲、乙、丙三套装置中,选取合理的组成部分(A、B、C、D、E、F、G),组装一套你认为更完善的实验装置,连接顺序(按气流从左到右的方向)为 ;在此装置及甲、乙、丙三装置中,你认为是否还缺少必要的装置,并说明原因
。
(3)如果反应前加入了m g Ca(OH)2,反应结束并冷却后倒出固体物质称量为n g(设反应中产生的水仍留在固体物质中)。则该固体物质中Ca(ClO)2的质量分数的表达式为(不必化简): 。