题目内容
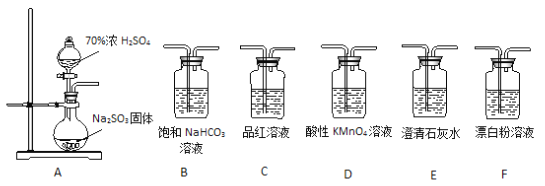
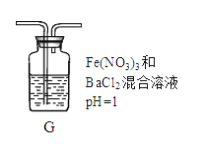
【题目】实验室制备硝基苯的反应原理和实验装置如下:

存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯,有关数据如表:
物质 | 熔点/℃ | 沸点/℃ | 密度/ g·cm-3 | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
浓硝酸 | 83 | 1.4 | 易溶于水 | |
浓硫酸 | 338 | 1.84 | 易溶于水 |
实验步骤如下:
取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合液,将混合酸小心加入B中,把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀,在50~60 ℃下发生反应,直至反应结束。

将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5% NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210 ℃馏分,得到纯硝酸基苯18 g。回答下列问题:
(1)装置B的名称是___________,装置C的作用是____________________。
(2)配制混合液时,________(填“能”或“不能”)将浓硝酸加入到浓硫酸中,说明理由:____________________________________________。
(3)为了使反应在50~60 ℃下进行,常用的方法是____________。
(4)在洗涤操作中,第二次水洗的作用是_____________________。
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140 ℃,应选用空气冷凝管,不选用直形冷凝管的原因是________________________________。
(6)本实验所得到的硝基苯产率是______________________________。
【答案】 分液漏斗 冷凝回流、平衡气压 不能 容易发生迸溅 水浴加热 洗去残留的NaOH及生成的盐 以免直形冷凝管通水冷却时导致温差过大而发生炸裂 72%
【解析】(1)根据仪器构造可判断装置B的名称是分液漏斗;硝酸和苯的沸点都较低,易挥发,装置C是冷凝管,所以装置C的作用是冷凝回流、平衡气压,增大反应物的转化率;(2)配制混合酸时,不能将浓硝酸加入到浓硫酸中,因为浓硝酸的密度低于浓硫酸,且浓硝酸的沸点较低,浓硫酸溶于水放出大量的热,若将浓硝酸加入到浓硫酸中,混合放出的热量使硝酸沸腾,导致液体迸溅;(3)为了使反应在50℃~60℃下进行,常用的方法是水浴加热,便于控制温度;(4)第一次水洗目的是除去过量酸,碱洗的目的也是除去剩余的酸,第二次水洗除去过量的氢氧化钠和生成的钠盐;(5)空气冷凝管一般适用沸点高于140℃的物质的蒸馏,硝基苯的沸点大于140℃,所以选择空气冷凝管,而不选择直形冷凝管,以免直形冷凝管通水冷却导致玻璃温差大而炸裂;(6)根据题意,硝酸的质量是15.2g,根据苯的质量控制,硝酸过量,按苯的质量计算理论生成硝基苯的质量是![]() ,实际得到硝基苯的质量是18.0g,所以硝基苯的产率是
,实际得到硝基苯的质量是18.0g,所以硝基苯的产率是![]() 。
。
点晴:对于设计给定条件下的物质制备方案这一类题目,在解答时一定要遵循物质制备方案设计的几条基本原则,对涉及的原料、基本化学反应原理、实验程序和仪器、设备等进行深入的研究,精心取舍,才能得出正确的答案。该类试题要求学生能够通过题给实验情境中适当迁移,准确把化学实验基础知识和基本操作技能运用到某些类似的实验中去,解决一些原理和操作较简单的问题,意在考查学生的实验技能和综合分析问题的能力。例如该题可以联系乙酸乙酯的制备、浓硫酸的稀释等相关实验。另外教材中也有相关硝基苯的制备实验,因此紧扣教材,掌握基础是解答好这类试题的关键。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案