题目内容
【题目】一定温度下,某容器中加入足量的碳酸钙,发生反应CaCO3(s) ![]() CaO(s)+CO2(g),达到平衡,下列说法正确的是
CaO(s)+CO2(g),达到平衡,下列说法正确的是
A. 将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度为原来的2倍
B. CaCO3(s)加热分解生成CaO(s)和CO2(g),△S<0
C. 将容器体积增大为原来的2倍,平衡向正反应方向移动
D. 保持容器体积不变,充入He,平衡向逆反应方向进行
【答案】C
【解析】试题分析:A.将体积缩小为原来的一半,当体系再次达到平衡时,若平衡不移动,CO2的浓度为原来的2倍,由于压强增大,平衡向着逆向移动,则平衡时二氧化碳的浓度小于原先的2倍,A错误;B.CaCO3(s)高温分解为CaO(s)和CO2(g),反应方程式为:CaCO3(s)![]() CaO(s)+CO2(g),反应生成气体,是熵值增加的过程,则△S>0,B错误;C.正反应是体积增大的可逆反应,将体积增大为原来的2倍,平衡将向正反应方向移动,C正确;D.保持容器体积不变,充入He,由于气体的浓度不变,则平衡不会移动,D错误;答案选C。
CaO(s)+CO2(g),反应生成气体,是熵值增加的过程,则△S>0,B错误;C.正反应是体积增大的可逆反应,将体积增大为原来的2倍,平衡将向正反应方向移动,C正确;D.保持容器体积不变,充入He,由于气体的浓度不变,则平衡不会移动,D错误;答案选C。

【题目】下表是A、B、C、D、E五种有机物的有关信息:
A | B | C | D | E |
①是一种烃,能使溴的四氯化碳溶液褪色 ②比例模型为:
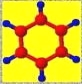
③能与水在一定条件下反应生成C | ①由C、H两种元素组成 ②球棍模型为:
| ①能与钠反应,但不能与NaOH溶液反应; ②能与E反应生成相对分子质量为100的酯 | ①由C、H、Br三种元素组成; ②相对分子质量为109 | ①由C、H、O三种元素组成; ②球棍模型为:
|
根据表中信息回答下列问题:
(1)写出A使溴的四氯化碳溶液褪色的化学方程式:__________________;
(2)A与氢气发生加成反应后生成分子F,F的同系物的通式为CnH2n+2。当n =________时,这类有机物开始有同分异构体。
(3)B的分子式为____________,写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:___ ;
(4)C与E反应能生成相对分子质量为100的酯,写出该反应的化学方程式:_____________。