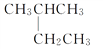��Ŀ����
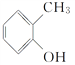
����Ŀ��FeCl3����;�㷺��
(1)ʵ��������FeCl3�Ʊ�Fe(OH)3���壺
��Fe(OH)3�����Ʊ���Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
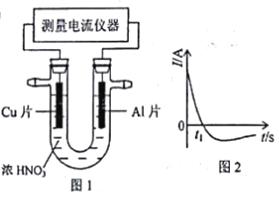
���������Ƶõ�Fe(OH)3�������ʵ�飺����װ��U�ι��ڣ���ʯī���缫��ͨ��һ��ʱ�����
___________���������ĺ��ɫ��������_________________________________
����Fe(OH)3�����м�H2SO4��Һ��������������_______________________________��
(2)FeCl3��Һ�����ڸ�ʴͭӡˢ��·�壬�÷�Ӧ�����ӷ���ʽΪ_________________________��
(3)FeCl3�����ھ�ˮ�������ӷ���ʽ��ʾ��ԭ��____________________________________��
(4)FeCl3��Һ��������FeCl2������FeCl2���Լ�Ϊ________________________��
(5)��FeCl3��Һ���ɲ����յõ��Ĺ���ɷ�Ϊ__________________��
(6)��֪Fe(OH)3��Ksp��8��10��38��ij��Һ��c(FeCl3)=0.05mol/L,���ҪʹFe(OH)3������ȫ��pH����Ϊ______________________��
(��Һ������Ũ��С��10-5mol/L��Ϊ��������ȫ,��֪lg2=0.3 lg5=0.7)
���𰸡� FeCl3+3H2O![]() Fe(OH)3(����)+3HCl �� Fe(OH)3���������� �Ȳ������ɫ������������ܽ� 2Fe3++Cu=Cu2++2Fe2+ Fe3++3H2O
Fe(OH)3(����)+3HCl �� Fe(OH)3���������� �Ȳ������ɫ������������ܽ� 2Fe3++Cu=Cu2++2Fe2+ Fe3++3H2O ![]() Fe(OH)3+3H+ K3[Fe(CN)6]��Һ Fe2O3 3.3
Fe(OH)3+3H+ K3[Fe(CN)6]��Һ Fe2O3 3.3
��������(1)�����ü��ȴ�FeCl3ˮ���������������壬��Fe(OH)3�����Ʊ��Ļ�ѧ����ʽΪFeCl3+3H2O![]() Fe(OH)3(����)+3HCl��
Fe(OH)3(����)+3HCl��
�ڽ�����е�Ӿ���ʣ�ͨ��һ��ʱ��������Դ���������ĵ缫����������ɫ���˵���������ƶ���˵��Fe(OH)3���������磻
�ۼ���ϡ�����ǵ������Һ��������������������۳�����������ϡ���ᣬ���������������ܽ⣬�ʿ����Ȳ������ɫ������������ܽ⣻
(2)Fe3+�������Դ���Cu2+����FeCl3��Һ�����ڸ�ʴͭӡˢ��·�壬������Ӧ�����ӷ���ʽΪ2Fe3++Cu=Cu2++2Fe2+ ��
(3)FeCl3�����ھ�ˮ�������ܽ���ˮ��ˮ������Fe(OH)3���壬������Ӧ�����ӷ���ʽΪFe3++3H2O ![]() Fe(OH)3+3H+��
Fe(OH)3+3H+��
(4)��ѡ��K3[Fe(CN)6]��Һ����FeCl3��Һ��������FeCl2������������ɫ������
(5)FeCl3��ǿ�������Σ������������������ӣ���FeCl3��Һ����ʱ��������ˮ������Fe(OH)3��HCl�������¶ȴٽ�HCl�ӷ�������������Һʱ�õ��������������ʱ������������ֽ⣬��Ӧ����ʽΪ2Fe(OH)3![]() Fe2O3+3H2O���������յõ����Ǻ���ɫ����Fe2O3��
Fe2O3+3H2O���������յõ����Ǻ���ɫ����Fe2O3��
(6)����ʱ��Fe(OH)3��Ksp=8��10-38��Ҫʹ��Һ�е�Fe3+������ȫ����������Һ�е�c(Fe3+)��10-5molL-1��Ksp=c(Fe3+)c3(OH-)=10-5��c3(OH-)=8��10-38 ��
c(OH-)=![]() mol/L=2��10-11mol/L��c(H+)=
mol/L=2��10-11mol/L��c(H+)=![]() =5��10-4mol/L��pH=4-lg5=3.3��
=5��10-4mol/L��pH=4-lg5=3.3��

 ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
ȫ�ŵ�����Ԫ�ƻ�ϵ�д�