题目内容
已知下列数据:
2Fe(s)+O2(g) =2FeO(s) △H=-544kJ·mol-1
4Al(s)+3O2(g) =2Al2O3(s) △H=-3350kJ·mol-1
则2Al(s) +3FeO(s) =Al2O3(s) + 3Fe(s)的△H是
A.- 859 kJ·mol-1 B.+859 kJ·mol-1
C.-1403 kJ·mol-1 D.-2491 kJ·mol-1
A
【解析】略

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案|
下列说法正确的是: | |
| [ ] | |
A. |
在100℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) |
B. |
已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)·c(CO32-)=6.82×10-6 |
C. |
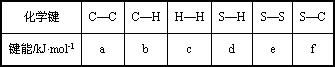
已知某些化学键的键能数据如下表:
则反应C3H7-S-S-C3H7(g)+3H2(g)=2C3H8(g)+2H2S(g)的焓变为ΔH=(2f+e+3c-2b-2d)kJ·mol-1 |
D. |
常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的pH减小 |
在相同温度下,体积均为1 L的四个密闭容器中,保持温度和容积不变,以四种不同的投料方式进行反应。平衡时有关数据如下(已知2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6 kJ·mol-1)。
2SO3(g)ΔH=-196.6 kJ·mol-1)。
|
容器 |
甲 |
乙 |
丙 |
丁 |
|
起始投料量 |
2 mol SO2+1 mol O2 |
1 mol SO2+0.5 mol O2 |
2 mol SO3 |
2 mol SO2+2 mol O2 |
|
反应放出或吸收的热量(kJ) |
a |
b |
c |
d |
|
平衡时c(SO3) (mol·L-1) |
e |
f |
g |
h |
下列关系正确的是( )
A.a=c;e=g B.a>2b;e>2f C.a>d;e>h D.c+98.3e>196.6
在相同温度和体积均为1L的四个密闭容器中,保持温度和容积不变,以四种不同的投料进行反应。平衡时有关数据如下
(已知相同条件下:2SO2+O2 2SO3 △H =-196.6kJ/mol)。
2SO3 △H =-196.6kJ/mol)。
|
容器 |
甲 |
乙 |
丙 |
丁 |
|
起始投入量 |
2molSO2+1molO2 |
1molSO2+0.5molO2 |
2molSO3 |
2molSO2+2molO2 |
|
反应放出或 吸收的热量(kJ) |
a |
b |
c |
d |
|
平衡时c(SO3)(mol/L) |
e |
f |
g |
h |
下列关系正确的是
A. a=c;e=g B. a>2b;e>2f C. a>d;e>h D. c+98.3e=196.6
 能源是人类生存和发展的重要支柱.研究和有效地开发新能源在能源紧缺的今天具有重要的理论意义.已知H2与CO反应生成CH3OH的过程如图所示:CO的燃烧热△H2=-bkJ?mol-1,CH3OH的燃烧热△H3=-ckJ?mol-1.请根据以上信息,回答下列有关问题:
能源是人类生存和发展的重要支柱.研究和有效地开发新能源在能源紧缺的今天具有重要的理论意义.已知H2与CO反应生成CH3OH的过程如图所示:CO的燃烧热△H2=-bkJ?mol-1,CH3OH的燃烧热△H3=-ckJ?mol-1.请根据以上信息,回答下列有关问题: