��Ŀ����
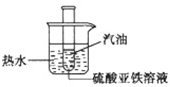 Na��FeSO4��Һ��Ӧ��һ����������ع۲쵽��Ӧȫ���̵��й�������������ͼ��ʾװ�ý���ʵ��Ľ����Ƚ��Թ������Ʊ���FeSO4��ҺҺ���ϸ���һ�������ͣ�Ȼ���Թܷ����ձ��У����Թ������Ͳ���ʧ�����Թ���Ͷ��һС���ƣ���Ѹ�����ϴ����ܵĵ�������
Na��FeSO4��Һ��Ӧ��һ����������ع۲쵽��Ӧȫ���̵��й�������������ͼ��ʾװ�ý���ʵ��Ľ����Ƚ��Թ������Ʊ���FeSO4��ҺҺ���ϸ���һ�������ͣ�Ȼ���Թܷ����ձ��У����Թ������Ͳ���ʧ�����Թ���Ͷ��һС���ƣ���Ѹ�����ϴ����ܵĵ�������
��1��ʵ�������͵�������______��
��2�������ƺ�۲쵽Һ�����д��������ݳ�����Һ����______ɫ�������ɣ�
��3��������Թ��м������ͺ�����Ͷ���������ܷ�����ը����ԭ����______��
��4��д������FeSO4��Һ��Ӧ�����ӷ���ʽ��______��
�ʴ�Ϊ������ʱ���������������Թ��ڿ����ž����𱣻������ã�
��2������ˮ��Ӧ�����������ƺ��������������ƺ�����������Ӧ����������������ɫ�������ʴ�Ϊ���ף�
��3���ƺ�ˮ��Ӧ�������ɵ����������ͣ����������ȼ�շ�����ը��
�ʴ�Ϊ������ˮ��Ӧ���ң���������������ʹ���ɵ�H2�����ͺ��Թ���Ŀ�����ϣ���ȼ�շ�����ը��
��4����Ӧ�����ӷ���ʽ��������ˮ��Ӧ�����ò�����������Һ��Ӧ���ۺϷ���д�����ӷ���ʽΪ��2Na+2H2O+Fe2+=2Na++Fe��OH��2��+H2����
�ʴ�Ϊ��2Na+2H2O+Fe2+=2Na++Fe��OH��2��+H2����
��������1�����͵��������ӷ����Թ��ڿ����Ͼ��������������ã�
��2������ˮ��Ӧ�����������ƺ��������������ƺ�����������Ӧ����������������ɫ������
��3���ƺ� ˮ��Ӧ�������ɵ����������ͣ����������ȼ�շ�����ը��
��4����Ӧ�����ַ���ʽ��������ˮ��Ӧ�����ò�����������Һ��Ӧ�ۺϷ���д�����ӷ���ʽ��
���������⿼�����ơ������仯�������ʵ�Ӧ�ã��������Ĺؼ�����ȷ������������Һ��Ӧ��ʵ��������ˮ��Ӧ�����ò�����������Һ��Ӧ��ͬʱע�ⷴӦ�����е�ijЩ����֪ʶ���練Ӧ���ȡ����������ȣ���Ŀ�Ѷ��еȣ�

 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�������ѧ֪ʶ������������⣺
��1����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼����ɵĹ��̡��������γɣ����1 mol��ѧ��ʱ�ͷţ������գ�����������֪������ȼ�ղ���P4O6�ķ��ӽṹ��ͼ��ʾ�����ṩ���¼��ܣ�kJ�� mol-1���� P��P��198�� P��O��360�� O��O��498������(P4)ȼ�յ��Ȼ�ѧ����ʽΪ ��
��2����ѧ�������֮������ת������Fe��Cu��C(ʯī)��CuSO4��Һ��FeSO4��Һ��Fe2(SO4)3��Һ ��AgNO3��ҺΪԭ�ϣ�ͨ��ԭ��ط�Ӧʵ��2Fe3+ + Cu��2Fe2+ + Cu2+,�������ͼ����������ʹ֮�γɱպϻ�·������Ԫ�ط��ű����缫���׳��е��Һ�� ��Һ���ҳ��е��Һ�� ��Һ����Ҫ�ס��������е����Ԫ������ʼ�ձ��ֲ��䣩
��3��ij�жԴ������м�⣬���ָ�����Ҫ��Ⱦ��Ϊ�����������PM2.5��ֱ��С�ڵ���2.5��m���������������Ҫ��ԴΪȼú��������β���ȡ���ˣ���PM2.5��SO2��NOx�Ƚ����о�������Ҫ���塣��ش��������⣺
�ٶ�PM2.5��������������ˮ�������Ƴɴ�������������ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±���
| ���� | K+ | Na+ | NH4+ | SO4���� | NO3�� | Cl�� |
| Ũ��/ mol?L-1 | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
����֪����������NO�ķ�ӦΪ��N2(g)+O2(g)
 2NO(g)
2NO(g) 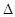 H��0
H��0��1 mol��������0.8 molN2��0.2 molO2,1300��ʱ���ܱ������ڷ�Ӧ�ﵽƽ�⡣���NOΪ8 �� 10-4 mol.������¶��µ�ƽ�ⳣ��K= ___________�����������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��ԭ���� ��