题目内容
在溴水中存在如下平衡:Br2+H2O
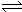
HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是( )
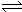
HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是( )
| A.加压 | B.加入NaOH |
| C.通入SO2气体 | D.通入HCl气体 |
A、加压对于没有气体参加的反应而言不会引起反应速率和化学平衡状态的改变,故A错误;
B、加入氢氧化钠,能和酸反应生成盐和水,所以产物的浓度减小,平衡正向移动,能使溴水的颜色变浅,故B正确;
C、通入SO2气体能和溴单质间发生氧化还原反应,使得溴单质的浓度减小,颜色变浅,故C正确;
D、通入HCl气体,相当于增大了氢离子的浓度,所以化学平衡逆向移动,溴单质的量增多,颜色加深,故D错误.
故选BC.
B、加入氢氧化钠,能和酸反应生成盐和水,所以产物的浓度减小,平衡正向移动,能使溴水的颜色变浅,故B正确;
C、通入SO2气体能和溴单质间发生氧化还原反应,使得溴单质的浓度减小,颜色变浅,故C正确;
D、通入HCl气体,相当于增大了氢离子的浓度,所以化学平衡逆向移动,溴单质的量增多,颜色加深,故D错误.
故选BC.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
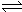 HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是( )
HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是( ) HBr+HBrO 当加入NaOH溶液后颜色变浅
HBr+HBrO 当加入NaOH溶液后颜色变浅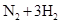
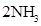 ,ΔH<0 为使氨的产率提高,理论上应采取低温高压的措施
,ΔH<0 为使氨的产率提高,理论上应采取低温高压的措施 HBr+HBrO 当加入NaOH溶液后颜色变浅
HBr+HBrO 当加入NaOH溶液后颜色变浅
 平衡体系增加压强使颜色变深
平衡体系增加压强使颜色变深

 ,△H<0 为使氨的产率提高,理论上应采取低温高压的措施
,△H<0 为使氨的产率提高,理论上应采取低温高压的措施