题目内容
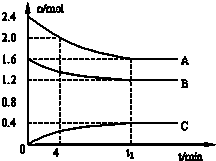
T℃时,A气体与B气体反应生成C气体.反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )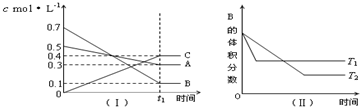

分析:由图(Ⅰ)可知,A和B的物质的量浓度减小,C的物质的量浓度增加,则A、B为反应物,C为生成物,由反应的浓度的变化之比等于化学计量数之比可得:△c(A):△c(B):△c(C)=0.2mol/L:0.6mol/L:0.4mol/L=1:3:2,则反应的化学方程式为A+3B 2C;
2C;
由图(Ⅱ)可知T1>T2,升高温度B的体积分数增大,说明生成温度平衡向逆反应方向移动,则正反应为放热反应,结合外界条件对平衡移动的影响解答该题.
 2C;
2C;由图(Ⅱ)可知T1>T2,升高温度B的体积分数增大,说明生成温度平衡向逆反应方向移动,则正反应为放热反应,结合外界条件对平衡移动的影响解答该题.
解答:解:由图(Ⅰ)可知,A和B的物质的量浓度减小,C的物质的量浓度增加,则A、B为反应物,C为生成物,由反应的浓度的变化之比等于化学计量数之比可得:△c(A):△c(B):△c(C)=0.2mol/L:0.6mol/L:0.4mol/L=1:3:2,则反应的化学方程式为A+3B 2C,则
2C,则
A.在(t1+10)min时,保持其他条件不变,增大压强,平衡向正反应方向移动,故A错误;
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向向逆反应方向移动,故B错误;
C.从等效平衡的角度考虑,T℃时,在相同容器中,若由0.3mol?L-1A、0.1 mol?L-1 B和0.4 mol?L-1 C反应,等效于0.5mol?L-1A、0.7 mol?L-1B,则为相同平衡状态,所以达到平衡后,
C的浓度仍为0.4 mol?L-1,故C正确;
D.由图(Ⅱ)可知T1>T2,升高温度B的体积分数增大,说明生成温度平衡向逆反应方向移动,则A的转化率减小,故D错误.
故选C.
 2C,则
2C,则A.在(t1+10)min时,保持其他条件不变,增大压强,平衡向正反应方向移动,故A错误;
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向向逆反应方向移动,故B错误;
C.从等效平衡的角度考虑,T℃时,在相同容器中,若由0.3mol?L-1A、0.1 mol?L-1 B和0.4 mol?L-1 C反应,等效于0.5mol?L-1A、0.7 mol?L-1B,则为相同平衡状态,所以达到平衡后,
C的浓度仍为0.4 mol?L-1,故C正确;
D.由图(Ⅱ)可知T1>T2,升高温度B的体积分数增大,说明生成温度平衡向逆反应方向移动,则A的转化率减小,故D错误.
故选C.
点评:本题考查化学平衡图象问题,题目难度较大,本题注意C项从等效平衡的角度分析,解答该题时注意分析图象的曲线变化特点,由图象得出反应的化学方程式为解答该题的关键.

练习册系列答案
相关题目
 T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.
T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示. C
C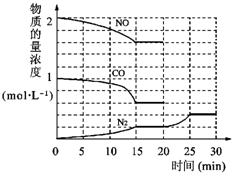 环境问题备受世界关注.化工厂以及汽车尾气排放的一氧化碳(CO)、氮氧化物(NOx)、硫化物等气体己成为大气污染的主要因素.
环境问题备受世界关注.化工厂以及汽车尾气排放的一氧化碳(CO)、氮氧化物(NOx)、硫化物等气体己成为大气污染的主要因素. O2+Hb?CO
O2+Hb?CO N2(g)+2CO2(g)△H=-113kJ?mol-1
N2(g)+2CO2(g)△H=-113kJ?mol-1 H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表: