题目内容
Al-AgO 电池性能优越,可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O,则下列说法正确的是


| A.AgO/Ag电极是负极 |
| B.当电极上析出1.08 g Ag时,电路中转移的电子为0.02mol |
| C.Al电极的反应式为:Al—3e-+4OH-= AlO2-+2H2O |
| D.在电解质溶液中OH-由Al电极移向AgO/Ag电极 |
BC
试题分析:电池总反应中铝元素由0升为+3价,发生氧化反应,说明Al电极是负极,而银元素由+1降为0价,发生还原反应,说明AgO/Ag电极是正极,故A错误;由于n=m/M,则正极上析出的Ag为0.01mol,由于2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O~6e一中各物质的系数之比等于物质的量之比,则电路中转移电子的物质的量为Ag的两倍,即0.02mol,故B正确;由总反应推断,负极主要反应物→产物是Al→AlO2一;由于化合价升高总数等于失去电子数,则Al—3e一→AlO2一;由于NaOH是强碱,应选择OH一使左右电荷总数相等,则Al—3e一+4OH一→AlO2一;由于左边比右边多4个H、2个O,说明生成物还有水,则Al电极的反应式为Al—3e一+4OH一=AlO2一+2H2O,故C正确;OH一是带负电的阴离子,原电池内电路中阴离子移向负极,则OH一应由AgO/Ag电极移向Al电极,故D错误。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
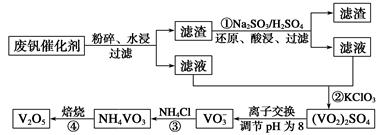
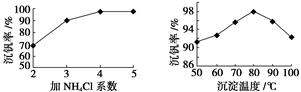
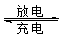 VO2++H2O+V3+,电池充电时阳极的电极反应式为 。
VO2++H2O+V3+,电池充电时阳极的电极反应式为 。 2PbSO4+2H2O。下列说法正确的是
2PbSO4+2H2O。下列说法正确的是 )是重要的能源物质,研究甲醇具有重要意义。
)是重要的能源物质,研究甲醇具有重要意义。 可制取甲醇,其反应为:
可制取甲醇,其反应为:

 的
的  晶体,在高温下它能传导
晶体,在高温下它能传导 离子。电池工作时正极反应为 。
离子。电池工作时正极反应为 。
 氧化成
氧化成 ,然后以
,然后以
 ,该过程中被氧化的元素是 ,当产生标准状况下2.24L
,该过程中被氧化的元素是 ,当产生标准状况下2.24L