题目内容
(11分)A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大;A有多种核素,其中一种没有中子;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4,A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不同的多种化合物。请回答下列问题:
(1) F在元素周期表中的位置是_______________;用电子式表示A与F两种元素组成的化合物的
形成过程______________________________________________。
已知下表中的数据是破坏1 mol物质中的化学键所吸收的能量(kJ),元素A的单质与元素F的单质在一定条件下反应生成2mol产物时释放的能量为____________kJ。
(2)用离子方程式表示E、F两种元素的非金属性强弱
还可以验证E、F两种元素非金属强弱的是(填写字母)
A.比较这两种元素的常见单质的沸点
B.比较这两种元素的单质与氢气化合的难易
C.比较这两种元素的最高价氧化物水化物的酸性
(3) A、C、E两两之间可形成甲、乙两种微粒,它们均为带一个单位负电荷的双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
(1) F在元素周期表中的位置是_______________;用电子式表示A与F两种元素组成的化合物的
形成过程______________________________________________。
已知下表中的数据是破坏1 mol物质中的化学键所吸收的能量(kJ),元素A的单质与元素F的单质在一定条件下反应生成2mol产物时释放的能量为____________kJ。
| 化学键 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
还可以验证E、F两种元素非金属强弱的是(填写字母)
A.比较这两种元素的常见单质的沸点
B.比较这两种元素的单质与氢气化合的难易
C.比较这两种元素的最高价氧化物水化物的酸性
(3) A、C、E两两之间可形成甲、乙两种微粒,它们均为带一个单位负电荷的双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
(第1空1分,其余空2分)
(1) 第三周期ⅦA族;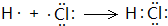 ;185
;185
(2)Cl2+S2-=2Cl-+S↓或Cl2+H2S=2H++2Cl-+S↓ ; BC
(3)HS-+OH-=S2-+H2O
(1) 第三周期ⅦA族;
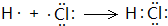 ;185
;185(2)Cl2+S2-=2Cl-+S↓或Cl2+H2S=2H++2Cl-+S↓ ; BC
(3)HS-+OH-=S2-+H2O
试题分析:A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,A有多种核素,其中一种没有中子,则A为H元素;B元素的最高价氧化物对应水化物与其氢化物能生成盐,则B为N元素;E元素原子的最外层电子数是其次外层电子数的3/4,最外层电子数为6,则E为S元素;D与A同主族,且与E同周期,则D为Na;A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的多种化合物,则C为O元素;F原子序数最大,则F为Cl元素;(1)F为Cl元素,在元素周期表中的位置是:第三周期ⅦA族;H与Cl两种元素组成的化合物为HCl,用电子式表示HCl的形成过程为:
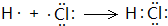 ,反应方程式为H2+Cl2=2HCl,反应生成2mol产物时释放的能量=2×432kJ-(436kJ+243kJ)=185kJ;(2)用离子方程式表示S、Cl两种元素的非金属性强弱为:Cl2+S2-=S↓+2Cl-,可以根据单质与氢气反应的难易程度及最高价氧化物对应水化物的酸性强弱比较非金属性强弱,单质沸点属于物理性质,不能比较非金属性强弱,故A错误,BC正确;(3)H、O、S形成的负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲为HS-,乙为OH-,离子反应为HS-+OH-=S2-+H2O。
,反应方程式为H2+Cl2=2HCl,反应生成2mol产物时释放的能量=2×432kJ-(436kJ+243kJ)=185kJ;(2)用离子方程式表示S、Cl两种元素的非金属性强弱为:Cl2+S2-=S↓+2Cl-,可以根据单质与氢气反应的难易程度及最高价氧化物对应水化物的酸性强弱比较非金属性强弱,单质沸点属于物理性质,不能比较非金属性强弱,故A错误,BC正确;(3)H、O、S形成的负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲为HS-,乙为OH-,离子反应为HS-+OH-=S2-+H2O。
练习册系列答案
相关题目

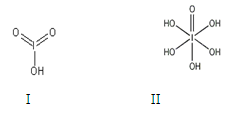


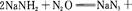
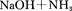
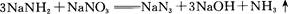 回答下列问题:
回答下列问题: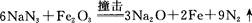
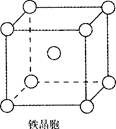
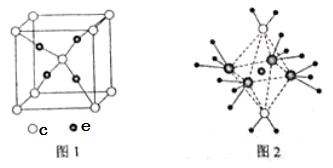
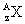 与
与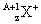 的两种微粒,下列叙述正确的是( )
的两种微粒,下列叙述正确的是( )