题目内容
合成氨的热化学方程式为:N2(g) + 3H2(g) 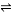 2NH3(g);△H = -92. 4 kJ/mol。现将1 mol N2 (g)、3 mol H2 (g) 充入一容积为2 L的密闭容器中,在500 ℃下进行反应,第10 min时达到平衡,NH3的体积分数为 ω,下列说法中正确的是:
2NH3(g);△H = -92. 4 kJ/mol。现将1 mol N2 (g)、3 mol H2 (g) 充入一容积为2 L的密闭容器中,在500 ℃下进行反应,第10 min时达到平衡,NH3的体积分数为 ω,下列说法中正确的是:
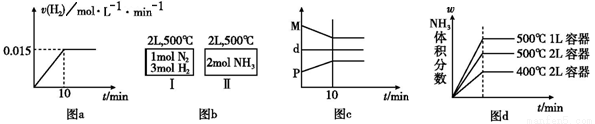
A. 若达到平衡时,测得体系放出9. 24 kJ热量,则H2反应速率变化曲线如图a所示
B. 如图b所示,容器Ⅰ和Ⅱ达到平衡时,NH3的体积分数为ω,则容器Ⅰ放出热量与容器Ⅱ吸收热量之和为92. 4 kJ
C. 反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为P,三者关系如图c
D. 若起始加入物料为1 mol N2、3 mol H2,在不同条件下达到平衡时,NH3的体积分数变化如图d所示
练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目



 CH3CHBrCH===CH2
CH3CHBrCH===CH2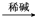 CH3CHOHCH2CHOCH3CHOHCH2CHO
CH3CHOHCH2CHOCH3CHOHCH2CHO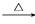 CH3CH===CHCHO+H2O
CH3CH===CHCHO+H2O B…
B…