题目内容
锡是一种银白色而又柔软的金属,2000年前人类就已开始使用锡.金属锡为排列在白金,黄金及银后面的第四种贵金属,它富有光泽、无毒、不易氧化变色,具有很好的杀菌、净化、保鲜效用.生活中常用于食品保鲜、罐头内层的防腐膜等.请回答下列有关锡的问题:
(1)锡在自然界几乎都以锡石的形式存在,此外还有极少量的锡的硫化物矿.以锡石(SnO2)为原料,用足量的焦炭作还原剂,在高温下可制得粗锡,该反应的化学方程式为________,粗锡经电解精炼可得纯锡,精炼时的阴极反应式为________.
(2)锡的氯化物有SnCl2和SnCl4.SnCl2是生产和化学实验中常用的还原剂,易发生水解;SnCl4常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃.
Ⅰ.若实验室中以SnCl2固体配制SnCl2溶液,试简述操作方法________.
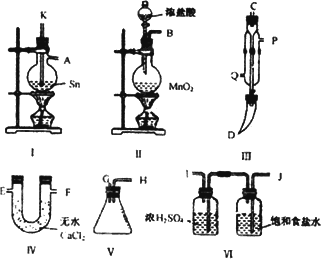
Ⅱ.某实验小组拟利用下图中的仪器,设计组装一套实验装置,用熔融的金属锡与干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热),已知金属锡的熔点为231℃.请回答下列各问题:
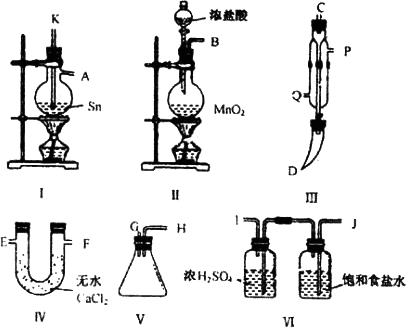
①用玻管(未画出)连接上述装置,正确的顺序是(填各接口的代码字母)________接________、________接________、________接________、________接________、________接________.
②装置Ⅵ的作用是________;装置Ⅳ的作用是________.
③冷凝管里冷却水的流向是从________进入,从________流出.
④试验时点燃Ⅰ处酒精灯,加热温度应大于________℃,待________即可停止加热.
⑤如果将制取的四氯化锡少许暴露于空气中,预期可看到的现象是________.
⑥该实验装置中还存在的一个问题是________.

 综合自测系列答案
综合自测系列答案