题目内容
已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):
H2(g)+Cl2(g)=2HCl(g) ΔH=-Q1 kJ/mol
H2(g)+Br2(g)=2HBr(g) ΔH=-Q2 kJ/mol
有关上述反应的叙述正确的是
H2(g)+Cl2(g)=2HCl(g) ΔH=-Q1 kJ/mol
H2(g)+Br2(g)=2HBr(g) ΔH=-Q2 kJ/mol
有关上述反应的叙述正确的是
| A.Q1<Q2 |
| B.生成物总能量均高于反应物总能量 |
| C.生成1molHCl气体时放出Q1热量 |
| D.1molHBr(g)具有的能量大于1molHBr(l)具有的能量 |
D
试题分析:A、因为Cl2比Br2活泼,Cl-Cl键能较大,放出的热量更多,应为Q1>Q2,因此A错误;B、两个反应都是放热反应,生成物的总能量低于反应物的总能量,故B错误;C、由热化学方程式可知,生成2mol氯化氢放出的热量才是Q1,故C错误;D、物质在气态时具有的能量一般高于液态和固态时,则1molHBr(g)具有的能量高于1molHBr(l)具有的能量,故D正确,答案选D。

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目

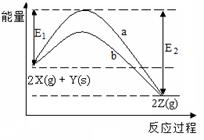
 2Z(g)的反应过程和能量关系图,下列说法正确的是( )
2Z(g)的反应过程和能量关系图,下列说法正确的是( )