题目内容
将0.2 mol下列烃完全燃烧后,生成的气体缓缓通过0.5 L 2mol/L的NaOH溶液中,生成正盐和酸式盐的物质的量之比为1:3,则该烷烃是( )
| A.乙烷 | B.丙烷 | C.丁烷 | D.戊烷 |
C
试题分析:假设该烷烃分子中含有n个C原子,则完全燃烧产生CO2的物质的量是0.2nmol。n(NaOH)=" 0.5" L ×2mol/L=1mol。假设产生的Na2CO3的物质的量为amol,则NaHCO3为3amol。则根据Na守恒可得2a+3a=1,解得a=0.2mol,所以Na2CO3为0.2mol,NaHCO3为0.6mol。根据C守恒可得0.2n=0.8,所以n=4.因此该烷烃是丁烷。

练习册系列答案
相关题目
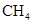 ,则相对分子质量最小的Y是甲醇
,则相对分子质量最小的Y是甲醇