题目内容
【题目】下列事实,不能用勒夏特列原理解释的是( )
A.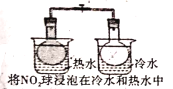 气体在热水中比在冷水中颜色深
气体在热水中比在冷水中颜色深
B.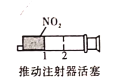 加压后气体颜色先变深后变浅
加压后气体颜色先变深后变浅
C.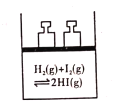 平衡体系加压后颜色变深
平衡体系加压后颜色变深
D.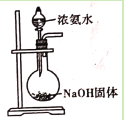 用浓氨水和NaOH固体制取氨气
用浓氨水和NaOH固体制取氨气
【答案】C
【解析】
A.2NO2![]() N2O4 是放热反应,温度升高平衡逆向移动,NO2浓度增大颜色加深,故在热水中比冷水中颜色深,此处是平衡的移动,能用勒夏特列原理解释,A项错误;
N2O4 是放热反应,温度升高平衡逆向移动,NO2浓度增大颜色加深,故在热水中比冷水中颜色深,此处是平衡的移动,能用勒夏特列原理解释,A项错误;
B.加压瞬间NO2浓度增大,颜色加深,后平衡正向移动,向生成N2O4方向移动,NO2浓度减小,故颜色变浅,B项错误;
C. I(g)+ H(g) ![]() 2HI(g),两边气体计量系数之和相等,加压平衡不移动,此处颜色加深是因为:加压体积缩小,碘单质的浓度增大了,与平衡移动无关, C项正确;
2HI(g),两边气体计量系数之和相等,加压平衡不移动,此处颜色加深是因为:加压体积缩小,碘单质的浓度增大了,与平衡移动无关, C项正确;
D. NH3(g)+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,加氢氧化钠固体就是增加OH-的浓度,化学平衡向左移动,释放出NH3,D项错误;
NH4++OH-,加氢氧化钠固体就是增加OH-的浓度,化学平衡向左移动,释放出NH3,D项错误;
答案选C。

【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
| C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯, 易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 易升华 | |
沸点/℃ | 132 | 173 | ||
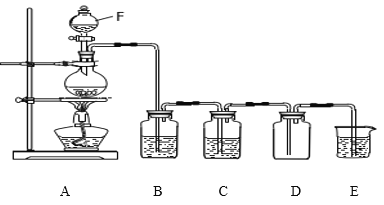
(1)用H2还原无水FeCl3制取FeCl2。有关装置如下:

①H2还原无水FeCl3制取FeCl2的化学方程式为_____________。
②按气流由左到右的方向,上述仪器的连接顺序为_________(填字母,装置可多次使用);C中盛放的试剂是_____________。
③该制备装置的缺点为________________。
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。

①仪器a的名称是__________。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是____,回收滤液中C6H5C1的操作方法是______。
③反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol/LNaOH溶液滴定,终点时消耗NaOH溶液为19.60 mL,则氯化铁的转化率为__________。
④为了减少实验误差,在制取无水FeCl2过程中应采取的措施有:________(写出一点即可)。
【题目】某温度下,反应H2(g)+CO2(g)![]() H2O(g)+CO(g)的平衡常数K=
H2O(g)+CO(g)的平衡常数K=![]() 。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示:
。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示:
甲 | 乙 | 丙 | |
c(H2)/(mol·L-1) | 0.010 | 0.020 | 0.020 |
c(CO2)/(mol·L-1) | 0.010 | 0.010 | 0.020 |
下列判断不正确的是( )
A. 反应开始时,丙容器中化学反应速率最大,甲容器中化学反应速率最小
B. 平衡时,乙容器中CO2的转化率大于60%
C. 平衡时,甲容器中和丙容器中H2的转化率均是60%
D. 平衡时,丙容器中c(CO2)是甲容器中的2倍,是 0.012 mol·L-1