��Ŀ����
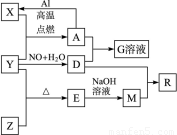
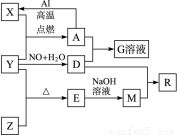
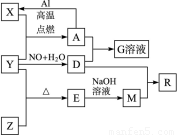
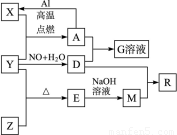
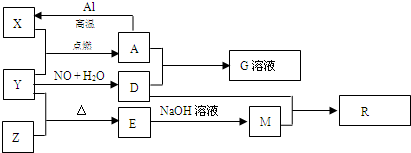
��֪X��Y��ZΪ���ʣ�����Ϊ���������YΪ���壬G��Һ�ʻ�ɫ��E�Dz�����ˮ�������������������ᷴӦ������֮���������ת����ϵ�����ֲ�������ȥ������ش��������⣺
��1��E�Ļ�ѧʽ��
��2��M��ˮ��Һ�׳�
��3��д��A��D��ϡ��Һ��Ӧ����G�����ӷ���ʽ
��4����2mol D��ϡ��Һ�У�����X��ĩ���������������ɵ�����ֻ��һ�֣���n��Xm+�������ֵΪ

��1��E�Ļ�ѧʽ��
SiO2
SiO2
����2��M��ˮ��Һ�׳�
ˮ����
ˮ����
������D��Ӧ�Ļ�ѧ����ʽΪNa2SiO3+2HNO3=H2SiO3��+2NaNO3
Na2SiO3+2HNO3=H2SiO3��+2NaNO3
����3��д��A��D��ϡ��Һ��Ӧ����G�����ӷ���ʽ
3Fe3O4+28H++NO3-=9Fe3++NO��+14H2O
3Fe3O4+28H++NO3-=9Fe3++NO��+14H2O
����4����2mol D��ϡ��Һ�У�����X��ĩ���������������ɵ�����ֻ��һ�֣���n��Xm+�������ֵΪ
0.75
0.75
��������X��Y��ZΪ���ʣ�����Ϊ�����E�Dz�����ˮ�������������������ᷴӦ����EΪ�������裬YΪ���嵥�ʣ�Y��Z��Ӧ���ɶ������裬��ZΪSi��YΪ����������������������������MΪ�����ƣ�G��Һ�ʻ�ɫ�����������ӣ���A�к���FeԪ�أ�X������Y�ڵ�ȼ����������A����XΪFe����AΪ���������������ת����ϵ��֪��DΪ���ᡢGΪ���������ݴ˽��
����⣺X��Y��ZΪ���ʣ�����Ϊ�����E�Dz�����ˮ�������������������ᷴӦ����EΪ�������裬YΪ���嵥�ʣ�Y��Z��Ӧ���ɶ������裬��ZΪSi��YΪ����������������������������MΪ�����ƣ�G��Һ�ʻ�ɫ�����������ӣ���A�к���FeԪ�أ�X������Y�ڵ�ȼ����������A����XΪFe����AΪ���������������ת����ϵ��֪��DΪ���ᡢGΪ��������
��1��������������֪��EΪSiO2���ʴ�Ϊ��SiO2��
��2��MΪ�����ƣ���ˮ��Һ�׳�ˮ�����������ᷴӦ����ʽΪ��Na2SiO3+2HNO3=H2SiO3��+2NaNO3��
�ʴ�Ϊ��ˮ������Na2SiO3+2HNO3=H2SiO3��+2NaNO3��
��3��A��D��ϡ��Һ��Ӧ����G�����ӷ���ʽΪ��3Fe3O4+28H++NO3-=9Fe3++NO��+14H2O��
�ʴ�Ϊ��3Fe3O4+28H++NO3-=9Fe3++NO��+14H2O��
��4����2mol HNO3��ϡ��Һ�У�����Fe��ĩ�������������������������ɵ�����ֻ��һ��ΪNO����Fe2+Ϊxmol�����ݵ���ת���غ㣬��n��NO��=
=
x mol�����ݵ�ԭ���غ��֪2n[Fe��NO3��2]+n��NO��=n��HNO3������2x mol+
x mol=2mol�����x=0.75���ʴ�Ϊ��0.75��
��1��������������֪��EΪSiO2���ʴ�Ϊ��SiO2��
��2��MΪ�����ƣ���ˮ��Һ�׳�ˮ�����������ᷴӦ����ʽΪ��Na2SiO3+2HNO3=H2SiO3��+2NaNO3��
�ʴ�Ϊ��ˮ������Na2SiO3+2HNO3=H2SiO3��+2NaNO3��
��3��A��D��ϡ��Һ��Ӧ����G�����ӷ���ʽΪ��3Fe3O4+28H++NO3-=9Fe3++NO��+14H2O��
�ʴ�Ϊ��3Fe3O4+28H++NO3-=9Fe3++NO��+14H2O��
��4����2mol HNO3��ϡ��Һ�У�����Fe��ĩ�������������������������ɵ�����ֻ��һ��ΪNO����Fe2+Ϊxmol�����ݵ���ת���غ㣬��n��NO��=
| 2x mol |
| 5-2 |
| 2 |
| 3 |
| 2 |
| 3 |
���������⿼�������ƶϡ����û�ѧ���������ԭ��Ӧ����ȣ��Ѷ��еȣ�G��Һ��ɫ��E���������ƶϵ�ͻ�ƿڣ��ٽ��ת����ϵ�������Ʒ������Ʒ������ƶϣ���4��ע�������غ㷨���м��㣮

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ