题目内容
将11.9g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g.另取等质量的合金溶于过量稀硝酸中,生成了6.72L NO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为( )A.22.1g
B.27.2g
C.30g
D.无法计算
【答案】分析:根据电子守恒计算出金属失去电子的物质的量,根据应中金属失去电子的物质的量等于生成碱的氢氧根离子的物质的量计算生成沉淀的质量.
解答:解:将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Mg2+离子,根据电子守恒,金属共失去电子的物质的量为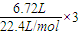 =0.9mol,
=0.9mol,
反应中金属失去电子的物质的量等于生成碱的氢氧根离子的物质的量,即n(OH-)=0.9mol,
所以反应后沉淀的质量等于11.9g+0.9mol×17g/mol=27.2g,
故选B.
点评:本题考查混合物的计算,题目难度不大,注意从守恒的角度做题较为简单.
解答:解:将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Mg2+离子,根据电子守恒,金属共失去电子的物质的量为
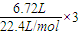 =0.9mol,
=0.9mol,反应中金属失去电子的物质的量等于生成碱的氢氧根离子的物质的量,即n(OH-)=0.9mol,
所以反应后沉淀的质量等于11.9g+0.9mol×17g/mol=27.2g,
故选B.
点评:本题考查混合物的计算,题目难度不大,注意从守恒的角度做题较为简单.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目