题目内容
【题目】下列溶液中与50 mL 1 mol·L-1的AlCl3溶液中氯离子浓度相等的是:
A. 150 mL 1 mol·L-1 的NaCl B. 75 mL 2 mol·L-1 的NH4Cl
C. 150 mL 3 mol·L-1 的KCl D. 75 mL 2 mol·L-1 的CaCl2
【答案】C
【解析】题目要求是氯离子的浓度相等,50 mL 1 molL-1的AlCl3溶液中氯离子浓度为3mol/L,所以应该选择氯离子浓度也是3mol/L的溶液。A为1mol/L,B为2mol/L,C为3mol/L,D为4mol/L,C正确。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】利用如图装置制取ClO2 , 并以ClO2为原料制备亚氯酸钠(NaClO2是一种高效氧化剂、漂白剂).已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO23H2O,高于38℃时析出晶体是NaClO2 , 高于60℃时NaClO2分解成NaClO3和NaCl. 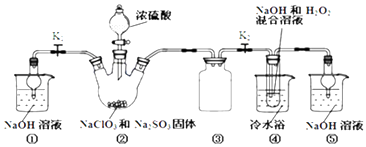
完成下列填空:
(1)装置②中产生ClO2的化学方程式为;装置④中发生反应的离子方程式为 .
(2)装置③的作用是;装置①和⑤在本实验中的作用 .
(3)装置④反应后的溶液中还含有少量NaOH杂质,从该溶液获得无水NaClO2晶体的操作步骤为:①减压,55℃左右蒸发结晶;②趁热过滤;③用50℃左右的温水洗涤;④低于60℃干燥,得到成品.步骤③中用50℃左右的温水洗涤的原因是 .
(4)亚氯酸钠纯度测定:①准确称取所得亚氯酸钠样品10.0g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应.将所得混合液配成250mL待测溶液.②取25.00mL待测液,用2.0 molL﹣1Na2S2O3标准液滴定(I2+2S2O32﹣=2I﹣+S4O62﹣),以淀粉溶液做指示剂,达到滴定终点时的现象为 . 重复滴定3次,测得数据如表所示,则该样品中NaClO2的质量分数为 .
实验序号 | 滴定前读数/mL | 滴定后读数/mL |
1 | 0.00 | 19.96 |
2 | 3.26 | 23.30 |
3 | 1.10 | 23.40 |
(5)实验过程中若NaClO2变质可分解为NaClO3和NaCl.取等质量NaClO2 , 其中一份加热高于60℃使之变质,另一份严格保存,均配成溶液,并分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量(填“相同”“不相同”或“无法判断”).
【题目】下列对应关系正确的是
选项 | 现象或事实 | 解释或结论 |
A | CuSO4+H2S===CuS↓+H2SO4 | 该反应不能发生,因为酸性H2SO4>H2S |
B | 向氯化钙溶液中通入CO2,未出现白色沉淀 | CO2过量,生成碳酸氢钙 |
C | 用激光笔照射向硅酸纳溶液中滴入几滴稀盐酸,有丁达尔现象 | 生成了硅酸胶体 |
D | 向某溶液中先滴加氯水再滴加KSCN,溶液变红 | 溶液中含有Fe2+ |
A. A B. B C. C D. D