题目内容
乙烯和苯是来自石油和煤的两种重要化工原料.请回答:
(1)乙烯通入溴的四氯化碳溶液中,观察到的现象是
 .
.
(2)乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
工艺一:CH2=CH2+Cl2+Ca(OH)2→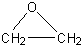 +CaCl2+H2O
+CaCl2+H2O
工艺二:2CH2=CH2+O2
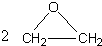
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,上述工艺一的原子利用率
(3)苯也是一种重要的化工原料,但人们对苯的认识经历了一个不断深化的过程.苯的分子式为
 ,称为凯库勒式,但后来大量实验事实和理论研究都表明,苯分子中6个碳原子之间的键是
,称为凯库勒式,但后来大量实验事实和理论研究都表明,苯分子中6个碳原子之间的键是
 .
.
(1)乙烯通入溴的四氯化碳溶液中,观察到的现象是
溶液褪色
溶液褪色
;其反应方程式为CH2=CH2+Br2→BrCH2CH2Br
CH2=CH2+Br2→BrCH2CH2Br
;乙烯在一定条件下发生加聚反应的化学方程式为

(2)乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
工艺一:CH2=CH2+Cl2+Ca(OH)2→
 +CaCl2+H2O
+CaCl2+H2O工艺二:2CH2=CH2+O2
| Ag |

根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,上述工艺一的原子利用率
低
低
;工艺二的原子利用率为100%
100%
.因此,在实际生产中,应采用工艺二
二
更环保、更经济.(3)苯也是一种重要的化工原料,但人们对苯的认识经历了一个不断深化的过程.苯的分子式为
C6H6
C6H6
.由于苯与同碳原子数的己烷相比,高度缺氢,人们认为它是一种不饱和烃,1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,其结构式为

完全相同的
完全相同的
.因此用凯库勒式表示苯的结构式是不确切的,只是沿用至今而已.苯能发生取代反应,请写出苯与液溴发生取代反应的化学方程式

分析:(1)乙烯与溴水发生加成反应,溴水褪色,乙烯可发生加聚反应生成聚乙烯;
(2)工艺一制取副产物多,原子利用率低;工艺二原子利用率为100%,原子利用率高;
(3)1个苯分子中含6个C和6个H,6个C之间的化学键完全相同,苯与溴发生取代反应生成溴苯和HBr.
(2)工艺一制取副产物多,原子利用率低;工艺二原子利用率为100%,原子利用率高;
(3)1个苯分子中含6个C和6个H,6个C之间的化学键完全相同,苯与溴发生取代反应生成溴苯和HBr.
解答:解:(1)乙烯与溴水发生加成反应,该反应为CH2=CH2+Br2→BrCH2CH2Br,观察到溶液褪色,乙烯可发生加聚反应生成聚乙烯,该反应为 ,故答案为:溶液褪色;CH2=CH2+Br2→BrCH2CH2Br;
,故答案为:溶液褪色;CH2=CH2+Br2→BrCH2CH2Br; ;
;
(2)工艺一除生成环氧乙烷外还有CaCl2和H2O的生成,副产物多,原子利用率低;而工艺二乙烯和氧气反应全部生成了环氧乙烷,原子利用率为100%,原子利用率高,所以在实际生产中,应采用工艺二,故答案为:低;100%;二;
(3)1个苯分子中含6个C和6个H,其分子式为C6H6,1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,结构式为 ,而大量实验事实和理论研究都表明,苯分子中6个碳原子之间的键完全相同,苯与溴发生取代反应生成溴苯和HBr,该反应为
,而大量实验事实和理论研究都表明,苯分子中6个碳原子之间的键完全相同,苯与溴发生取代反应生成溴苯和HBr,该反应为 ,
,
故答案为:C6H6; ; 完全相同的;
; 完全相同的; .
.
 ,故答案为:溶液褪色;CH2=CH2+Br2→BrCH2CH2Br;
,故答案为:溶液褪色;CH2=CH2+Br2→BrCH2CH2Br; ;
;(2)工艺一除生成环氧乙烷外还有CaCl2和H2O的生成,副产物多,原子利用率低;而工艺二乙烯和氧气反应全部生成了环氧乙烷,原子利用率为100%,原子利用率高,所以在实际生产中,应采用工艺二,故答案为:低;100%;二;
(3)1个苯分子中含6个C和6个H,其分子式为C6H6,1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,结构式为
 ,而大量实验事实和理论研究都表明,苯分子中6个碳原子之间的键完全相同,苯与溴发生取代反应生成溴苯和HBr,该反应为
,而大量实验事实和理论研究都表明,苯分子中6个碳原子之间的键完全相同,苯与溴发生取代反应生成溴苯和HBr,该反应为 ,
,故答案为:C6H6;
 ; 完全相同的;
; 完全相同的; .
.点评:本题考查有机物的结构与性质,侧重苯和乙烯的结构与性质的考查,把握苯中的特殊结构及化学键为解答的关键,注意加成反应、取代反应的差别,题目难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
下列说法中错误的是( )
| A、甲烷是最简单的有机化合物 | B、乙烯和苯是来自石油和煤的两种基本化工原料 | C、乙醇和乙酸都是常用调味品的主要成分 | D、食物中的营养物质包括糖类、油脂、蛋白质 |