题目内容
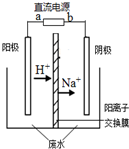 最近有研究人员发现了一种处理高浓度乙醛废水的新方法-隔膜电解法,乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法正确的是( )
最近有研究人员发现了一种处理高浓度乙醛废水的新方法-隔膜电解法,乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法正确的是( )分析:A.a为正极,b为负极,负极发生氧化反应,通入甲烷;
B.钠离子和硫酸根离子不参与电极反应,物质的量不变;
C.质量不守恒;
D.阳极发生4OH--4e-═O2↑+2H2O、CH3CHO-2e-+H2O=CH3COOH+2H+,阴极发生4H++4e-=2H2↑、CH3CHO+2e-+2H2O═CH3CH2OH+2OH-.
B.钠离子和硫酸根离子不参与电极反应,物质的量不变;
C.质量不守恒;
D.阳极发生4OH--4e-═O2↑+2H2O、CH3CHO-2e-+H2O=CH3COOH+2H+,阴极发生4H++4e-=2H2↑、CH3CHO+2e-+2H2O═CH3CH2OH+2OH-.
解答:解:A.a为正极,b为负极,连接电解池阴极的是原电池负极,负极上燃料失电子发生氧化反应,该燃料电池中燃料是甲烷,所以b电极上投放的是CH4,故A错误;
B.钠离子和硫酸根离子不参与电极反应,物质的量不变,故B错误;
C.质量不守恒,应为CH3CHO-2e-+H2O=CH3COOH+2H+,故C错误;
D.阳极发生4OH--4e-═O2↑+2H2O、CH3CHO-2e-+H2O=CH3COOH+2H+,阴极发生4H++4e-=2H2↑、CH3CHO+2e-+2H2O═CH3CH2OH+2OH-,则两极除分别生成乙酸和乙醇外,均产生了无色气体,则阳极产生的是O2,故D正确.
故选D.
B.钠离子和硫酸根离子不参与电极反应,物质的量不变,故B错误;
C.质量不守恒,应为CH3CHO-2e-+H2O=CH3COOH+2H+,故C错误;
D.阳极发生4OH--4e-═O2↑+2H2O、CH3CHO-2e-+H2O=CH3COOH+2H+,阴极发生4H++4e-=2H2↑、CH3CHO+2e-+2H2O═CH3CH2OH+2OH-,则两极除分别生成乙酸和乙醇外,均产生了无色气体,则阳极产生的是O2,故D正确.
故选D.
点评:本题考查了原电池和电解池的原理,侧重于学生的分析能力的考查,为高频考点,注意把握反应的原理和电极方程式的书写,为解答该题的关键,难度中等.

练习册系列答案
相关题目