题目内容
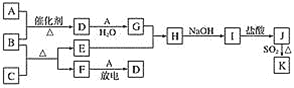
【题目】从有机含碘(含I2、ICl等)废水中回收碘并制备KI溶液的一种工艺流程如下:
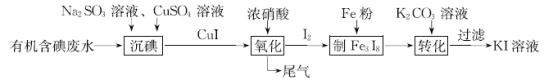
下列说法错误的是
A.“沉碘”时,Na2SO3作还原剂
B.“氧化”时,尾气可用NaOH溶液吸收处理
C.“制Fe3I8”时,每生成1 mol Fe3I8转移8mole-
D.“转化”时,K2CO3溶液可用K2SO4溶液代替
【答案】D
【解析】
A. “沉碘”时,Na2SO3将I2、ICl还原为I-,作还原剂;I-再与Cu2+作用,生成I2和CuI,A正确;
B. “氧化”时,尾气为氮的氧化物,可用NaOH溶液吸收处理,B正确;
C. “制Fe3I8”时,I由-1价升高到0价,每生成1 mol Fe3I8转移8mole-,C正确;
D. “转化”时,K2CO3溶液提供碱性环境,将Fe3+、Fe2+都转化为沉淀,这是K2SO4溶液所不能替代的,D错误。
故选D。

 阅读快车系列答案
阅读快车系列答案【题目】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为 Cu2S,含少量 Fe2O3、SiO2 等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
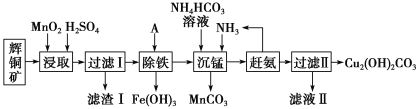
已知:
①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
② Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除适当增加硫酸浓度外,还可采取的措施有__________(任写一种)。
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的化学方程式:______________。
(3)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为_________,若加 A 后溶液的 pH调为4.0,则溶液中 Fe3+的浓度为_________mol/L。
(4)写出“沉锰”(除 Mn2+)过程中反应的离子方程式:_________________________。
(5)“赶氨”时,最适宜的操作方法是________________。
(6)过滤Ⅱ得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是________________。