题目内容
【题目】Ⅰ.现有x g某气体,它由三原子分子构成,它的摩尔质量为M gmol-1.若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为_____个。
(2)该气体在标准状况下的体积为______L。
(3)一个该气体分子的质量______g。
Ⅱ.(1)等物质的量的CO和CO2其原子数之比为 ______。
(2)同温、同压下,A、B两容器分别充满O2和O3 ,则O2和O3的密度之比为______,若两容器中O2和O3 所含原子总数相等,则A容器和B容器的容积比是______。
【答案】![]()
![]()
![]() 2:32:33:2。
2:32:33:2。
【解析】
I.根据n=![]() 、V=n×Vm、n=
、V=n×Vm、n=![]() 及分子构成计算;II.(1).根据分子的构成判断;(2).根据阿伏加德罗定律及其推论判断。
及分子构成计算;II.(1).根据分子的构成判断;(2).根据阿伏加德罗定律及其推论判断。
I.(1). 现有x g某气体,它由三原子分子构成,它的摩尔质量为M gmol-1,该气体的物质的量为:![]() =
=![]() mol,所含原子的物质的量为3×
mol,所含原子的物质的量为3×![]() mol=
mol=![]() mol,原子总数为
mol,原子总数为![]() mol×NAmol-1=
mol×NAmol-1=![]() ,故答案为:
,故答案为:![]() ;
;
(2).该气体在标准状况下的体积为![]() mol×22.4L/mol=
mol×22.4L/mol=![]() L,故答案为:
L,故答案为:![]() ;
;
(3).根据摩尔质量的定义可知,1mol该气体的质量为M g,即NA个该气体分子的质量为M g,则一个该气体分子的质量为:![]() g,故答案为:
g,故答案为:![]() ;
;
II.(1).1mol CO分子中含有2mol原子,1mol CO2分子中含有3mol原子,则等物质的量的CO和CO2其原子数之比为2:3,故答案为:2:3;
(2).同温同压下,气体的密度之比等于其相对分子质量之比,即![]() =
= ![]() =2:3;若两容器中O2和O3 所含原子总数相等,则O2和O3的物质的量之比为3:2,在同温同压下,气体的体积之比等于其物质的量之比,即A容器和B容器的容积比也是3:2,故答案为:2:3;3:2。
=2:3;若两容器中O2和O3 所含原子总数相等,则O2和O3的物质的量之比为3:2,在同温同压下,气体的体积之比等于其物质的量之比,即A容器和B容器的容积比也是3:2,故答案为:2:3;3:2。

【题目】SO2的防治与利用对于环境保护意义重大。某小组在实验室中对SO2的性质及回收利用等相关问题进行探究。
(1)用下图装置制备纯净的SO2,发生装置中反应的化学方程式为________,装置的连接顺序为:a→________(按气流方向,用小写字母表示)
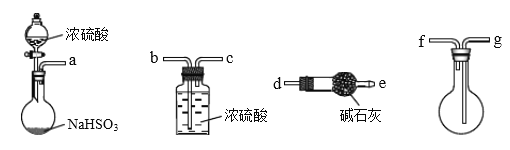
(2)用如图装置探究SO2的性质。限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、 淀粉-KI溶液、新制H2S溶液。

操作步骤 | 实验现象 | 解释原因 |
用注射器将新制H2S溶液注入充满SO2的烧瓶 | 产生乳白色浑浊 | +4价S有_______性 |
用注射器将_______溶液注入充满SO2的烧瓶 | _______ | +4价S有还原性,反应的离子方程式为_______ |
(3)工业上回收利用SO2的一种途径是:
![]()
该小组在实验室探究步骤Ⅱ时,一定条件下向100mL c0mol·L-1的(NH4)2SO3溶液通入空气后,欲测定溶液中(NH4)2SO3的氧化率(α)。
①为该小组设计实验方案(不必描述操作过程的细节,物理量的数值用字母表示):______________________________________________________________________________
②α =________×100%(用实验方案中的物理量表示)。
