题目内容
某物质A的产量可以用来衡量一个国家的石油化工发展水平。其 与水加成的产物B是一种常用的有机溶剂,在生活中有重要的应用。
(1)A的电子式为________,B的分子式为________。
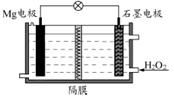
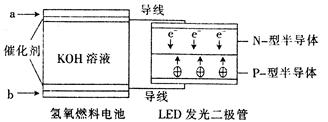
若用B与O2制成燃料电池,并以稀硫酸溶液为电解质溶液,回答(2)-(5)题:
(2)负极上的电极反应式为_______________________________________。
(3)消耗标准状况下的5.6 L O2时,有__________mol电子发生转移。
(4)开始放电时,正极附近溶液的pH__________(填“增大”、“减小”或“不变”);
(5)溶液中H+由___________区向__________区移动(填“正极”或“负极”)。
(1)A的电子式为________,B的分子式为________。
若用B与O2制成燃料电池,并以稀硫酸溶液为电解质溶液,回答(2)-(5)题:
(2)负极上的电极反应式为_______________________________________。
(3)消耗标准状况下的5.6 L O2时,有__________mol电子发生转移。
(4)开始放电时,正极附近溶液的pH__________(填“增大”、“减小”或“不变”);
(5)溶液中H+由___________区向__________区移动(填“正极”或“负极”)。
(1)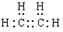 ;分子式 C2H6O (各1分)
;分子式 C2H6O (各1分)
(2)C2H6O -12e- +3H2O =12H+ +2CO2 ↑ (3分) (3) 1 (1分)
(4)增大 (1分) (5) 负极 正极 ( 各1分)
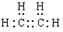 ;分子式 C2H6O (各1分)
;分子式 C2H6O (各1分)(2)C2H6O -12e- +3H2O =12H+ +2CO2 ↑ (3分) (3) 1 (1分)
(4)增大 (1分) (5) 负极 正极 ( 各1分)
试题分析:(1)某物质A的产量可以用来衡量一个国家的石油化工发展水平,可知A为乙烯, 电子式为
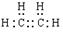 ;与水加成的产物B是一种常用的有机溶剂,则B为乙醇。则答案为分子式 C2H6O 。
;与水加成的产物B是一种常用的有机溶剂,则B为乙醇。则答案为分子式 C2H6O 。(2)若用B与O2制成燃料电池,并以稀硫酸溶液为电解质溶液,由乙醇燃料电池发生的氧化还原反应可知乙醇失去电子,则在负极上发生失电子反应C2H6O -12e- +3H2O =12H+ +2CO2 ↑ 。(3)根据电子守恒,当消耗5.6 L O2时,即0.25mol氧气反应了,转移1mol电子。(4)开始放电时,正极反应中有氢离子参加了反应,故附近溶液的pH增大。(5)溶液中H+由负极区向正极区移动。

练习册系列答案
相关题目