题目内容
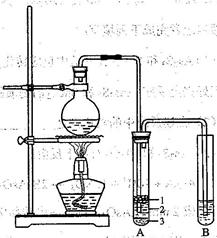
实验室制乙烯通常采用乙醇与浓硫酸(体积比为1:3)混合加热到170℃制得,反应过程中乙醇常被炭化,溶液中有黑色物质出现,随着反应进行炭化现象越来越严重,同时制得的乙烯气体中通常会含有CO2、SO2等气体,为确认混合气体中含有乙烯和二氧化硫,可让混合气体依次通过如图实验装置.(可供选择的试剂:品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾溶液、浓硫酸,试剂可重复使用.)
A.①②中盛放的试剂分别为①______;②______;(填试剂名称)
B.能说明二氧化硫气体存在的现象是______.
C.能确认含有乙烯的现象是______.
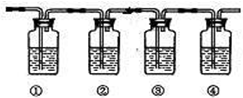
A.①②中盛放的试剂分别为①______;②______;(填试剂名称)
B.能说明二氧化硫气体存在的现象是______.
C.能确认含有乙烯的现象是______.

制得的乙烯气体中通常会含有CO2、SO2等气体,为确认混合气体中含有乙烯和二氧化硫,利用二氧化硫具有漂白性,乙烯可以使溴水或高锰酸钾溶液褪色,但检验乙烯前,需要把二氧化硫全部除去,一般用氢氧化钠溶液吸收,吸收后用品红溶液检验是否除净;试剂选择为品红试液检验二氧化硫存在、氢氧化钠溶液吸收二氧化硫、品红试液检验二氧化硫是否除净、高锰酸钾溶液褪色检验乙烯的存在;
A依据分析判断试剂的选择是①品红,②NaOH溶液,
故答案为:品红;NaOH溶液;
B能说明二氧化硫气体存在的现象是装置①中品红褪色,
故答案为:装置①中品红褪色;
C能确认含有乙烯的现象是装置③中品红不褪色,装置④中高锰酸钾溶液褪色,
故答案为:装置③中品红不褪色,装置④中溶液褪色;
A依据分析判断试剂的选择是①品红,②NaOH溶液,
故答案为:品红;NaOH溶液;
B能说明二氧化硫气体存在的现象是装置①中品红褪色,
故答案为:装置①中品红褪色;
C能确认含有乙烯的现象是装置③中品红不褪色,装置④中高锰酸钾溶液褪色,
故答案为:装置③中品红不褪色,装置④中溶液褪色;

练习册系列答案
相关题目
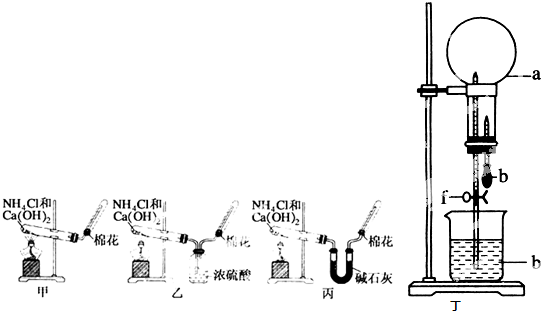
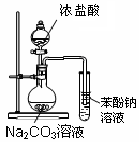
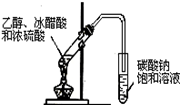
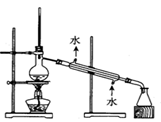
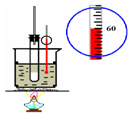
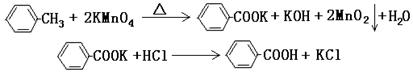
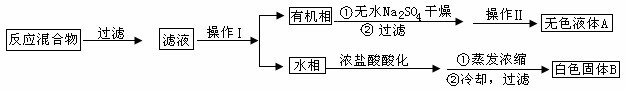

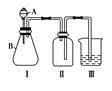 (4)该兴趣小组同学共同设计了如图所示的实验装置,利用装置Ⅰ、Ⅱ制取气体,请回答下列问题:
(4)该兴趣小组同学共同设计了如图所示的实验装置,利用装置Ⅰ、Ⅱ制取气体,请回答下列问题: