题目内容
将2.56 g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应中消耗HNO3的物质的量为( )
| A.0.05 mol | B.1 mol | C.1.05 mol | D.0.13 mol |
D
解析试题分析:有题意知,n(Cu)=0.04mol,n(g)=0.05mol,铜刚开始和硝酸反应生成NO2气体,随着反应的进行,硝酸变稀,反应生成NO气体,硝酸既表现氧化性,又表现酸性,表现氧化性的硝酸转化成气体,根据氮原子守恒,表现氧化性的硝酸为0.05mol, 表现酸性的硝酸生成硝酸铜,物质的量为0.08mol,共计0.13mol,D正确。
考点:考查硝酸的计算

练习册系列答案
相关题目
高岭土中[Al2(Si2O5)(OH)4]中SiO2的质量分数为
| A.46.5% | B.23.3% | C.21.7% | D.35.7% |
下列叙述正确的是
| A.二氧化硅是酸性氧化物,不与任何酸反应 |
| B.因为CO2通入水玻璃中可制得硅酸,说明碳酸的酸性比硅酸酸性强 |
| C.SiO2晶体中,每个硅原子与两个氧原子相连 |
| D.工业上制玻璃的主要原料有:黏土、石灰石、石英 |
二氧化硅(SiO2)又称硅石,是制备硅及其化合物的重要原料(见下图)。下列说法正确的是( )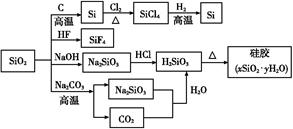
| A.SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物 |
| B.SiO2和Si都是光导纤维材料 |
| C.在硅胶中加入CoCl2可显示硅胶吸水是否失效 |
| D.图中所示转化反应都是非氧化还原反应 |
下列有关硫及其化合物的说法正确的是( )
| A.浓硫酸具有吸水性,因而能使蔗糖碳化 |
| B.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
| C.在反应SO2+2H2S=3S+2H2O中SO2作氧化剂 |
| D.硫粉在过量的纯氧中燃烧可以生成SO3 |
氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是( )。
| A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
| B.通常状况下,干燥的氯气能与Fe反应 |
| C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照H2和Cl2的混合气体时,因迅速化合而爆炸 |
| D.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸 |
二氧化氯(ClO2)是一种广谱、高效的消毒剂,易溶于水,尤其在水处理等方面有广泛应用。以下是某校化学研究小组设计实验室制取ClO2的工艺流程图。下列有关说法正确的是 ( )。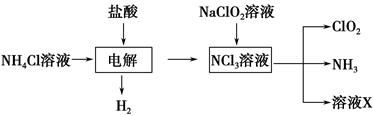
A.电解时发生反应的化学方程式为2HCl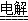 Cl2↑+H2↑ Cl2↑+H2↑ |
| B.由NaClO2溶液制取0.6 mol ClO2时,至少消耗0.1 mol NCl3 |
| C.将产生的混合气体通过盛有碱石灰的干燥器以除去ClO2中的NH3 |
| D.溶液X的主要成分为NaClO2和NaOH |
下列化学物质在实际生产生活和科技等方面的应用不正确的是 ( )。
| A.测定NaOH熔点时,可以将NaOH放入石英坩埚中高温加热 |
| B.石英砂可以用于制取高纯度的硅,硅是将太阳能转化为电能的常用材料 |
| C.因为氨易液化,液氨在气化时会吸收大量的热量,所以液氨可作制冷剂 |
| D.硫酸和硝酸都是重要的工业原料,工业上可用于制化肥、农药和炸药 |
如图是某煤发电厂处理废气的装置示意图。下列说法中错误的是( )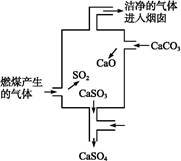
| A.使用此废气处理装置可减少酸雨的形成 |
| B.装置内发生的反应有化合、分解和置换反应 |
C.整个过程的反应可表示为:2SO2+2CaCO3+O2 2CaSO4+2CO2 2CaSO4+2CO2 |
| D.可用酸性高锰酸钾溶液检验废气处理是否达标 |