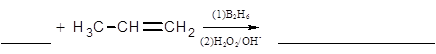题目内容
(1)B;A。
(2)不会,因在冷凝管中被冷却成液体回流到圆底烧瓶中
(3)催化和吸水作用 防止液体暴沸。
(4)因反应可逆,增加一种反应物的量可提高另一种成本较高的异戊醇的转化率。
(5)洗去乙酸和硫酸,洗去可能残存的少量酸。
解析试题分析:冷凝管竖直放置时,进水方向与蒸气流向一致;圆底烧瓶中的物质不会从上口跑掉,因为在冷凝管中蒸气会被冷却成液体回流到圆底烧瓶中;浓H2SO4在此反应中起催化剂和吸水作用,碎瓷片防止液体暴沸;由于酯化反应是可逆反应,增加乙酸的量可提高异戊醇的转化率;③中用蒸馏水洗涤,目的是除去乙酸和硫酸,④中洗去可能残存的少量酸。
考点:有机物的制备和分离提纯实验设计与评价。

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
乙酸乙酯是一种用途广泛的精细化工产品。某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:
已知:①氯化钙可与乙醇形成CaCl2·6C2H5OH
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
③2CH3CH2OH
 CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O I.制备过程
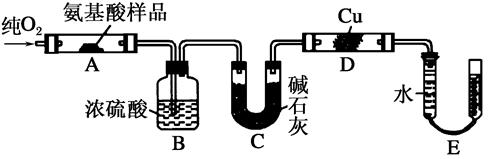
装置如图所示,A中放有浓硫酸,B中放有9.5mL无水乙醇和6mL冰醋酸,D中放有饱和碳酸钠溶液。
(1)写出乙酸与乙醇发生酯化反应的化学方程式 。
(2)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是 (填入正确选项前的字母)
A.25mL B.50mL C.250mL D.500mL
(3)球形干燥管的主要作用是 。
(4)预先向饱和Na2CO3溶液中滴加几滴酚酞试液,目的是
。
Ⅱ.提纯方法:①将D中混合液转入分液漏斗进行分液。
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤。有机层倒入一干燥的烧瓶中,用无水硫酸镁干燥,得粗产物。
③将粗产物蒸馏,收集77.1℃的馏分,得到纯净干燥的乙酸乙酯。
(5)第①步分液时,选用的两种玻璃仪器的名称分别是 、 。
(6)第②步中用饱和食盐水、饱和氯化钙溶液、最后用水洗涤,分别主要洗去粗产品中的 , , 。
已知①CH3CH2OH CH2=CH2↑+H20
CH2=CH2↑+H20
CH2=CH2+Br2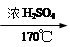 BrCH2—CH2Br
BrCH2—CH2Br
②乙醇、1,2-二溴乙烷、乙醚的有关物理性质如下表所示。
| | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 通常状况下的状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 熔点/℃ | -130 | 9 | -116 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
某化学小组拟用乙醇、溴等为原料在实验室制备少量的1,2一二溴乙烷,实验装置如右图所示(装置A中的加热部分的仪器装置省略没有画出)。
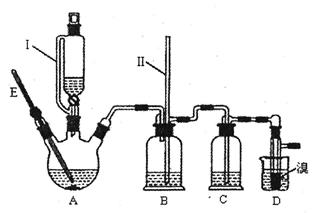
(1)仪器E的名称是 。
(2)仪器Ⅰ是漏斗,其左部的玻璃管的作 用是 (填字母)。
a.使漏斗中液体容易滴下
b.有利于吸收气体杂质
c.防止A中三颈烧瓶里的液体爆沸
(3)实验时,A中三颈烧瓶里放入几片碎瓷片的目的是 。加热反应过程中,三颈烧瓶里除生成乙烯外,还可能生成的有机副产物主要是 。
(4)反应过程中,若B中长玻璃导管(Ⅱ)里的液面上升,则说明可能是由于 (填“D中出现堵塞”或“C中杂质已除尽”)造成的。
(5)反应过程中,D中需用冷水冷却盛有液溴的试管,其主要目的是 。说明制备1,2-二溴乙烷的反应已经结束的实验现象是 。
下列叙述错误的是( )
| A.乙烯和苯都能使溴水褪色,褪色的原因相同 |
| B.淀粉、油脂、蛋白质都能水解,但水解产物不同 |
| C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| D.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |