题目内容
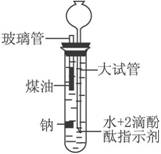
有人设计出一种在隔绝空气条件下让钠与FeSO4溶液反应的方法以验证反应实质。实验时,往100 mL大试管中先加40 mL煤油,取3粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入FeSO4溶液使煤油的液面至胶塞,并夹紧弹簧夹(如右图)。仔细观察,回答下列问题:
(1)有关钠的现象:____________ ____________ 。
(2)大试管中溶液颜色的变化:____________ 。
(3)装置中液面的变化:大试管内____________;长颈漏斗内____________。
(4)写出钠与硫酸亚铁反应的离子方程式:________________________ 。
解析:(1)金属Na与FeSO42-溶液反应实质是Na先与水反应,使Na粒熔化,并随气泡的生成而在两种液体界面处上下跳动。
(2)因反应生成的NaOH又与FeSO42-反应生成白色絮状沉淀,溶液的颜色逐渐变浅。(3)因产生了H2,使装置内压强增大,故大试管内液面下降,长漏斗内液面上升。
(4)2Na+2H2O+Fe2+=Fe(OH)2↓+H2↑+2Na+
答案:
(1)有气泡生成,钠粒熔化成小球,且在煤油和FeSO42-溶液界面处上下跳动,最终完全溶解
(2)下层溶液中出现白色絮状沉淀,溶液的颜色逐渐变浅
(3)下降上升
(4)2Na+2H2O+Fe2+=Fe(OH)2↓+H2↑+2Na+

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
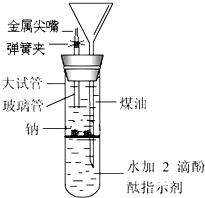 有人设计出一种在隔绝空气下让钠与水反应的方法,利用煤油来控制反应速率.使学生能仔细观察到各种实验现象.该方法简便、安全、现象明显、有趣味性.实验装置如图所示,将规格为6×55mm玻璃管和长颈漏斗插入橡皮孔中,玻璃管外套上30mm的乳胶管,乳胶管上再接规格为6×30mm金属尖嘴管,乳胶管上夹上弹簧夹.
有人设计出一种在隔绝空气下让钠与水反应的方法,利用煤油来控制反应速率.使学生能仔细观察到各种实验现象.该方法简便、安全、现象明显、有趣味性.实验装置如图所示,将规格为6×55mm玻璃管和长颈漏斗插入橡皮孔中,玻璃管外套上30mm的乳胶管,乳胶管上再接规格为6×30mm金属尖嘴管,乳胶管上夹上弹簧夹.