题目内容
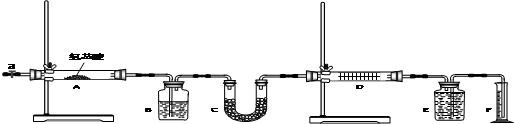
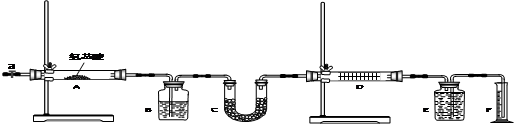
I.实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成.取w g该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.现用图示装置进行实验(铁架台、铁夹、酒精灯等未画出)请回答下列有关问题:
(1)写出装置D中分别盛放的试剂:D
(2)检查装置气密性,进行如下操作后A中氨基酸开始反应,请用序号表示正确的操作顺序
(3)样品氨基酸充分燃烧后,待E装置气体冷却至室温后记录F装置的液面读数,请指出读数时应注意的问题:
(4)通过该实验所能测定的数据,能否确定该氨基酸的分子式:
II.室温下,将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到了蓝色沉淀.为了确定沉淀的组成,某研究性学习小组进行了以下试验和研究.
(1)【提出假说】
假设一:两者反应只生成CuCO3沉淀;
假设二:两者反应只生成Cu(OH)2沉淀;
假设三:
(2)【理论探究】
查阅资料:CuCO3和Cu(OH)2均不带结晶水;KSP〔CuCO3〕=1.4×10-10
KSP〔Cu(OH)2〕=5.6×10-20若只由此数据结合适当计算来判断,最有可能正确的是假设
(3)【实验探究】
步骤一:将CuSO4溶液倒入等浓度等体积的Na2CO3溶液中并搅拌,有蓝色沉淀生成.
步骤二:将沉淀从溶液中分离出来,其操作方法为:①过滤,②
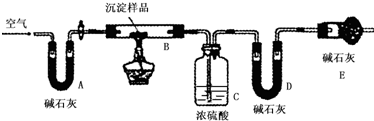
步骤三:利用下图所示装置,进行定量分析:
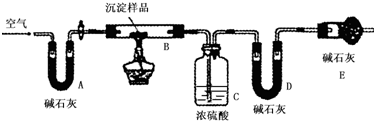
①A装置中玻璃仪器的名称是U 形管.
②仪器组装好后首先要进行的实验操作是
③实验结束时通入过量的空气的作用是保证装置中的水蒸气和CO2被C、D装置完全吸收.
④数据记录:
(4)【实验结论】
利用上述数据初步判断该沉淀的成分是CuCO3和Cu(OH)2,在沉淀中二者的物质的量之比为

(1)写出装置D中分别盛放的试剂:D
铜网
铜网
;(2)检查装置气密性,进行如下操作后A中氨基酸开始反应,请用序号表示正确的操作顺序
③④②③①
③④②③①
.(实验操作:①使用酒精灯加热A处;②使用酒精灯加热D处;③打开活塞a,通入氧气; ④关闭活塞a,记录F装置的液面读数.)(3)样品氨基酸充分燃烧后,待E装置气体冷却至室温后记录F装置的液面读数,请指出读数时应注意的问题:
读数时视线应与刻度线和凹液面最低点相切,移动量筒使E和F装置的液面相平
读数时视线应与刻度线和凹液面最低点相切,移动量筒使E和F装置的液面相平
.(4)通过该实验所能测定的数据,能否确定该氨基酸的分子式:
不能
不能
.II.室温下,将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到了蓝色沉淀.为了确定沉淀的组成,某研究性学习小组进行了以下试验和研究.
(1)【提出假说】
假设一:两者反应只生成CuCO3沉淀;
假设二:两者反应只生成Cu(OH)2沉淀;
假设三:
生成的是CuCO3和Cu(OH)2的混合物
生成的是CuCO3和Cu(OH)2的混合物
;(2)【理论探究】
查阅资料:CuCO3和Cu(OH)2均不带结晶水;KSP〔CuCO3〕=1.4×10-10
KSP〔Cu(OH)2〕=5.6×10-20若只由此数据结合适当计算来判断,最有可能正确的是假设
二
二
.(3)【实验探究】
步骤一:将CuSO4溶液倒入等浓度等体积的Na2CO3溶液中并搅拌,有蓝色沉淀生成.
步骤二:将沉淀从溶液中分离出来,其操作方法为:①过滤,②
洗涤
洗涤
,③干燥.步骤三:利用下图所示装置,进行定量分析:

①A装置中玻璃仪器的名称是U 形管.
②仪器组装好后首先要进行的实验操作是
检查装置的气密性
检查装置的气密性
.③实验结束时通入过量的空气的作用是保证装置中的水蒸气和CO2被C、D装置完全吸收.
④数据记录:
(4)【实验结论】
利用上述数据初步判断该沉淀的成分是CuCO3和Cu(OH)2,在沉淀中二者的物质的量之比为
1:1
1:1
.若所得沉淀是纯净物而不是混合物,请写出该物质的化学式Cu2(OH)2CO3
Cu2(OH)2CO3
.| B装置的质量(g) | C装置的质量(g) | D装置的质量(g) | |
| 实验前 | 15.4 | 262.1 | 223.8 |
| 试验后 | 6.1 | 264.8 | 230.4 |
分析:I、氨基酸燃烧生成N2、CO2和H2O,H2O(g)被B瓶中浓H2SO4吸收,CO2被C管中碱石灰吸收,D管中Cu网可以吸收未反应的O2.这样,进入E瓶的只有N2,排入F量筒中水的体积就是生成的N2的体积.测出生成的CO2、H2O(g)的质量及N2的体积,确定分子中三种元素原子个数比,由此确定最简式.再结合氨基酸相对分子质量可求氨基酸的分子式.
(1)为保证氨基酸完全燃烧需通过量的氧气,利用铜网和氧气在加热条件下反应除去未反应完氧气,以防止影响N2的体积的测定.
(2)先排除装置内空气,以免影响氮气体积测定,然后先加热铜网防止通入的氧气为反应而被收集,再通入氧气,加热氨基酸样品燃烧.
(3)保证内外压强相等,读数时应注意移动量筒使E和F装置的液面相平;视线应与刻度线和凹液面最低点相切.
(4)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素的质量,据此可以确定其原子个数比,确定其最简式.若要确定分子式还需测定该氨基酸的相对分子质量.
II.(1)根据Cu(OH)2和CuCO3都不溶于水猜测.
(2)根据溶度积估算相同铜离子浓度要沉淀需碳酸根浓度、氢氧根浓度.
(3)将沉淀从溶液中分离出来,其操作步骤一般为:①过滤,②洗涤,③干燥.
实验通过加热沉淀分解根据浓硫酸及碱石灰的增重确定沉淀的成分,仪器组装好后首先要进行的实验操作是检查装置的气密性.
(4)装置B内剩余的物质为氧化铜,装置C内盛放浓硫酸,吸收生成的水,根据装置C增重,确定生成水的质量;
装置D内盛放碱石灰,吸收生成的二氧化碳,根据装置D增重,确定生成二氧化碳质量;根据C原子、H原子守恒计算CuCO3和Cu(OH)2,在沉淀中二者的物质的量之比,并由此确定.
(1)为保证氨基酸完全燃烧需通过量的氧气,利用铜网和氧气在加热条件下反应除去未反应完氧气,以防止影响N2的体积的测定.
(2)先排除装置内空气,以免影响氮气体积测定,然后先加热铜网防止通入的氧气为反应而被收集,再通入氧气,加热氨基酸样品燃烧.
(3)保证内外压强相等,读数时应注意移动量筒使E和F装置的液面相平;视线应与刻度线和凹液面最低点相切.
(4)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素的质量,据此可以确定其原子个数比,确定其最简式.若要确定分子式还需测定该氨基酸的相对分子质量.
II.(1)根据Cu(OH)2和CuCO3都不溶于水猜测.
(2)根据溶度积估算相同铜离子浓度要沉淀需碳酸根浓度、氢氧根浓度.
(3)将沉淀从溶液中分离出来,其操作步骤一般为:①过滤,②洗涤,③干燥.
实验通过加热沉淀分解根据浓硫酸及碱石灰的增重确定沉淀的成分,仪器组装好后首先要进行的实验操作是检查装置的气密性.
(4)装置B内剩余的物质为氧化铜,装置C内盛放浓硫酸,吸收生成的水,根据装置C增重,确定生成水的质量;
装置D内盛放碱石灰,吸收生成的二氧化碳,根据装置D增重,确定生成二氧化碳质量;根据C原子、H原子守恒计算CuCO3和Cu(OH)2,在沉淀中二者的物质的量之比,并由此确定.
解答:解:I、(1)为保证氨基酸完全燃烧需通过量的氧气,利用铜网和氧气在加热条件下反应除去未反应完氧气,以防止影响N2的体积的测定,
故答案为:铜网;
(2)先排除装置内空气,以免影响氮气体积测定,然后先加热铜网防止通入的氧气为反应而被收集,再通入氧气,加热氨基酸样品燃烧,
故答案为:③④②③①;
(2)装置B内盛放浓硫酸,吸收生成的水,根据装置B增重,确定Wg该种氨基酸中含氢元素质量,装置C内盛放碱石灰,吸收生成的二氧化碳,根据装置C增重,确定Wg该种氨基酸中含碳元素质量,故答案为:H元素;O元素;
(3)利用排水法测定氮气的体积,确定Wg该种氨基酸中含氮元素质量.读氮气体积时应注意上下移动乙管,使甲、乙两管液面相平,以保证管内压强应与外界大气压相等,视线应与凹液面最低处相平,
故答案为:读数时视线应与刻度线和凹液面最低点相切,移动量筒使E和F装置的液面相平;
(4)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素的质量,据此可以确定其原子个数比,确定其最简式.若要确定分子式还需测定该氨基酸的相对分子质量,
故答案为:不能;
II.(1)Cu(OH)2和CuCO3都不溶于水,可能为二者混合物,
故答案为:生成的是CuCO3和Cu(OH)2的混合物;
(2)令铜离子的浓度为cmol/L,则铜离子开始沉淀时,所需碳酸根的浓度c(CO32-)=
.
铜离子开始沉淀时,所需氢氧根的浓度c(OH-)=
=
×10-10.碳酸钠溶液呈碱性c(OH-)>10-7,
所以最可能沉淀的是氢氧化铜,
故答案为:二;
(3)将沉淀从溶液中分离出来,过滤后需洗涤表面附着的一些可溶性物质.其操作步骤一般为:①过滤,②洗涤,③干燥.
实验通过加热沉淀分解根据浓硫酸及碱石灰的增重确定沉淀的成分,仪器组装好后首先要进行的实验操作是检查装置的气密性.
故答案为:步骤二:洗涤; 步骤三:②检查装置的气密性;
(4)由表可知水的质量为264.8g-262.1g=2.7g,物质的量为
=0.15mol,由H原子守恒可知氢氧化铜为0.15mol.二氧化碳的质量为230.4g-223.8g=6.6g,物质的量为
=0.15mol,由C原子守恒可知碳酸铜为0.15mol.
所以CuCO3和Cu(OH)2的物质的量之比为1:1.
所得沉淀是纯净物而不是混合物,则其化学式为 Cu2(OH)2CO3.
故答案为:1:1; Cu2(OH)2CO3.
故答案为:铜网;
(2)先排除装置内空气,以免影响氮气体积测定,然后先加热铜网防止通入的氧气为反应而被收集,再通入氧气,加热氨基酸样品燃烧,
故答案为:③④②③①;
(2)装置B内盛放浓硫酸,吸收生成的水,根据装置B增重,确定Wg该种氨基酸中含氢元素质量,装置C内盛放碱石灰,吸收生成的二氧化碳,根据装置C增重,确定Wg该种氨基酸中含碳元素质量,故答案为:H元素;O元素;
(3)利用排水法测定氮气的体积,确定Wg该种氨基酸中含氮元素质量.读氮气体积时应注意上下移动乙管,使甲、乙两管液面相平,以保证管内压强应与外界大气压相等,视线应与凹液面最低处相平,
故答案为:读数时视线应与刻度线和凹液面最低点相切,移动量筒使E和F装置的液面相平;
(4)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素的质量,据此可以确定其原子个数比,确定其最简式.若要确定分子式还需测定该氨基酸的相对分子质量,
故答案为:不能;
II.(1)Cu(OH)2和CuCO3都不溶于水,可能为二者混合物,
故答案为:生成的是CuCO3和Cu(OH)2的混合物;
(2)令铜离子的浓度为cmol/L,则铜离子开始沉淀时,所需碳酸根的浓度c(CO32-)=
| 1.4×10-10 |
| c |
铜离子开始沉淀时,所需氢氧根的浓度c(OH-)=
|
|
所以最可能沉淀的是氢氧化铜,
故答案为:二;
(3)将沉淀从溶液中分离出来,过滤后需洗涤表面附着的一些可溶性物质.其操作步骤一般为:①过滤,②洗涤,③干燥.
实验通过加热沉淀分解根据浓硫酸及碱石灰的增重确定沉淀的成分,仪器组装好后首先要进行的实验操作是检查装置的气密性.
故答案为:步骤二:洗涤; 步骤三:②检查装置的气密性;
(4)由表可知水的质量为264.8g-262.1g=2.7g,物质的量为
| 2.7g |
| 18g/mol |
| 6.6g |
| 44g/mol |
所以CuCO3和Cu(OH)2的物质的量之比为1:1.
所得沉淀是纯净物而不是混合物,则其化学式为 Cu2(OH)2CO3.
故答案为:1:1; Cu2(OH)2CO3.
点评:本题考查学生利用燃烧法确定有机物分子组成的知识,根据原子守恒法来解答,难度较大,关键在于理解实验原理.

练习册系列答案
相关题目