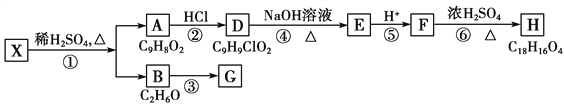
题目内容
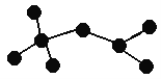
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
A. 原子半径:Z>W>X>Y
B. 元素X、Z的最高化合价分别与其主族序数相等
C. 最高价氧化物对应水化物的酸性:Y>X>W
D. 最简单气态氢化物的热稳定性:Y>X>W>Z
【答案】C
【解析】W原子的质子数是其最外层电子数的三倍,说明W是磷,相应地X、Y、Z分别是氮、氧、硅。A. 同周期元素原子半径:Z>W,X>Y,同主族元素原子半径:W>X,总之,Z>W>X>Y,故A正确;B. 元素X、Z的最高化合价分别与其主族序数相等,故B正确;C. 因为氧不存在最高价氧化物对应水化物,故C错误;D. 非金属性:Y>X>W>Z,最简单气态氢化物的热稳定性:Y>X>W>Z,故D正确。故选C。

【题目】某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如下:
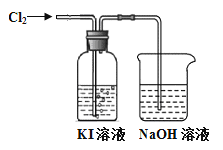
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)已知I2+I-![]() I3- , I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
I3- , I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
操作 | 实验现象 | |
a | 取2~3 mL黄色溶液,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色, 水层显浅黄色。 |
b | 取2~3 mL饱和碘水,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色,水层几近无色。 |
① 实验b的目的是 。
② 根据实验a中,水层中含有的粒子有 。
③ 实验a中水溶液颜色变浅的原因是 。
④ 为保证实验的严谨性,在实验a、b的基础上,需补充一个实验,该实验为 。
(2)通入氯气,溶液由黄色变为无色,是因为氯气将I2氧化。已知1 mol Cl2可氧化0.2 mol I2,该反应的化学方程式是 。
(3) 根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为 。