题目内容
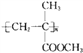
【题目】工程塑料ABS树脂的结构简式为: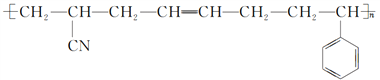 ,一种合成ABS树脂的路线如下:(A、B、S分别表示合成时的三种单体)
,一种合成ABS树脂的路线如下:(A、B、S分别表示合成时的三种单体)
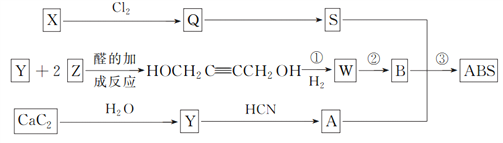
(1)写出Y和Z的结构简式:Y________,Z________。
(2)反应类型:反应②________;反应③________。
(3)事实上,工业上获得单体S是将X在高温下催化脱氢而制得的,催化剂多为Fe2O3等金属氧化物。
①试写出工业上获得S的化学方程式:______________________;
②与图示获得S相比,其优越性有_______________。
【答案】 CH≡CH HCHO 消去反应 加聚反应 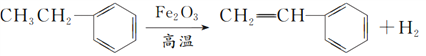 工序少,节省原料,污染小
工序少,节省原料,污染小
【解析】根据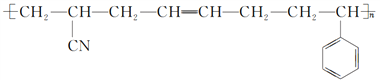 ,该高聚物的形成过程属于加聚反应,合成该高聚物的单体为:CH2=CH-CN、CH2=CH-CH=CH2、
,该高聚物的形成过程属于加聚反应,合成该高聚物的单体为:CH2=CH-CN、CH2=CH-CH=CH2、![]() ;根据流程图,CaC2与水反应生成CH≡CH,CH≡CH与HCN加成生成A,A为CH2=CH-CN;结合单体的结构可知,B为CH2=CH-CH=CH2,则W为HOCH2CH2CH2CH2OH,W发生羟基的消去反应生成B,Y+2Z发生醛的加成反应生成HOCH2C≡CCH2OH,Y为CH≡CH,则Z为HCHO;S为
;根据流程图,CaC2与水反应生成CH≡CH,CH≡CH与HCN加成生成A,A为CH2=CH-CN;结合单体的结构可知,B为CH2=CH-CH=CH2,则W为HOCH2CH2CH2CH2OH,W发生羟基的消去反应生成B,Y+2Z发生醛的加成反应生成HOCH2C≡CCH2OH,Y为CH≡CH,则Z为HCHO;S为![]() ,则X为乙苯(
,则X为乙苯(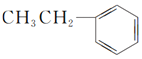 ),X发生侧链的取代反应生成Q(
),X发生侧链的取代反应生成Q(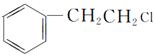 ),
),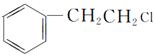 中的氯原子消去生成
中的氯原子消去生成![]() 。
。
(1)根据上述分析,Y和Z的结构简式分别为CH≡CH、HCHO,故答案为:CH≡CH;HCHO;
(2)反应②为羟基的消去反应;反应③为A、B、S分子间发生的加聚反应,故答案为:消去反应;加聚反应;
(3)事实上,工业上获得单体S(![]() )是将乙苯在高温下催化脱氢而制得的,催化剂多为Fe2O3等金属氧化物。
)是将乙苯在高温下催化脱氢而制得的,催化剂多为Fe2O3等金属氧化物。
①工业上由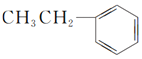 获得
获得![]() 的化学方程式为
的化学方程式为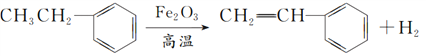 ,故答案为:
,故答案为: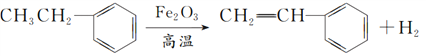 ;
;
②与图示获得S相比,其优越性有工序少,节省原料,污染小,故答案为:工序少,节省原料,污染小。

【题目】现有部分短周期元素的性质或原子结构如表:
元素编号 | 元素性质或原子结构 |
A | 有三个电子层,K,M层电子数之和等于L层电子数 |
B | 短周期中金属性最强 |
C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
D | 元素最高正价是+7价 |
(1)用化学用语回答下列问题:
①A元素在周期表中的位置;
②C单质分子的电子式;
③D的原子结构示意图;
④电子式表示A和B元素组成的化合物的形成过程: .
(2)元素D与元素A相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是(填选项序号).
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)X是由A,B,C,D四种元素中的某种元素组成的单质,能经图所示的过程转化为(其他条件略去). ![]()
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,无现象,然后滴加适量H2O2溶液,有白色沉淀生成,则该白色沉淀为 , 试写出Y与H2O2溶液反应的化学方程式:;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为 .
【题目】为除去某物质中所含的杂质,所选用的试剂或操作方法正确的是
序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
① | NaCl溶液 | Na2CO3 | 加入盐酸,蒸发 |
② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
④ | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
A. ①②③④
B. ②③④
C. ①③④
D. ①②③