题目内容
在50mL bmol·L-1的AlCl3溶液中加入50mL amol·L-1 NaOH溶液。
(1)当a、b满足_____________________条件时,无沉淀产生。
(2)当a、b满足_____________________条件时,先有沉淀生成,后又有部分沉淀溶解,此时Al(OH)3的质量为_____________________克。
(1)a≥4b (2)3b<a<4b; 3.9(4b-a)
解析试题分析:在AlCl3溶液中加入NaOH溶液时首先发生反应:AlCl3+3NaOH=Al(OH)3↓+3NaCl 。产生白色沉淀;当NaOH过量时发生反应:Al(OH)3+ OH-= AlO2-+ 2H2O 。沉淀又溶解。由方程式可看出n(OH-)<3n(Al3+)时,有白色沉淀,当n(OH-)=3n(Al3+)时,沉淀达到最大值。当4n(Al3+)>n(OH-)>3n(Al3+)时,沉淀逐渐溶解。当n(OH-)≥4n(Al3+)时,沉淀完全溶解。由于AlCl3溶液与NaOH溶液的体积相同,所以二者的浓度比就是二者的物质的量的比。(1)当a、b满足 a≥4b条件时,无沉淀产生。(2)当沉淀达到最大值时, n(Al(OH)3)=n(Al3+)=0.05mol.m(Al(OH)3)= 0.05mol×78g/mol=3.9g.当a、b满足3b<a<4b时,先有沉淀生成,后又有部分沉淀溶解,根据方程式Al(OH)3+ OH-= AlO2-+ 2H2O可知1mol的NaOH溶解1mol的Al(OH)3。所以此时Al(OH)3的质量为3.9(4b-a)g.
考点:考查AlCl3溶液与NaOH溶液反应产生的沉淀的质量关系的知识。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案元素周期表里金属元素和非金属元素分界线附近能找到
| A.制农药元素 | B.制催化剂元素 |
| C.制半导体元素 | D.制耐高温合金元素 |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.0.1 mol Cl2全部溶于水后转移电子的数目为0.1NA |
| B.标准状况下,0.56 L丙烷中含有共价键的数目为0.2NA |
| C.25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA |
| D.常温常压下,14 g C2H4、C3H6的混合气体中含有碳原子的数目为NA |
用NA表示阿伏加德罗常数,下列叙述正确的是 ( )
| A.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| B.0.5molC3H8分子中所含C-H共价键数为2NA |
| C.标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA |
D.1mol碳正离子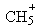 所含的电子数为11NA 所含的电子数为11NA |
用NA表示阿伏加德罗常数的值。下列叙述正确的是(相对原子质量:D-2 O-16 Cu-64)
| A.18 g的D216O中含有的中子数为9 NA |
| B.物质的量浓度均为1.0mol/L的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA |
| C.33.6 L NO2溶于足量的水得到的溶液中含有的NO3-数为NA |
| D.32 g铜发生氧化还原反应,一定失去NA个电子 |
下列两种气体的分子数一定相等的是
| A.质量相等、密度不同的N2和C2H4 |
| B.体积相等的CO和N2 |
| C.等温、等体积的O2和N2 |
| D.等压、等体积的N2和CH4 |
如图是某溶液在稀释过程中溶质的物质的量浓度随溶液体积的变化曲线图,根据图中数据分析可得出a值等于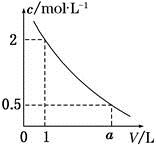
| A.2 | B.3 | C.4 | D.5 |
在100 g浓度为18 mol·L-1,密度为ρ(g·cm-3)的浓硫酸中加入一定量的水稀释成9 mol·L-1的硫酸,则加入水的体积为
| A.小于100 mL | B.等于100 mL |
| C.大于100 mL | D.小于 mL mL |
设NA为阿伏加德罗常数的值。下列说法正确的是( )。
| A.常温常压下,17 g甲基(—14CH3)所含的中子数为9 NA |
| B.标准状况下,11.2 L苯中含有的碳碳双键数为1.5 NA |
| C.42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3 NA |
| D.1 mol氯气与氢氧化钙溶液完全反应生成氯化钙和氯酸钙,转移的电子数为6 NA |