题目内容
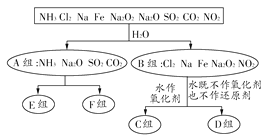
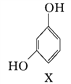
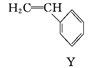
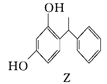
【题目】氢能源是21世纪极具开发前景的新能源之一,它既是绿色能源,又可循环使用。如图是氢能源循环体系图(X是H2O;Y是H2、O2)。回答下列问题:
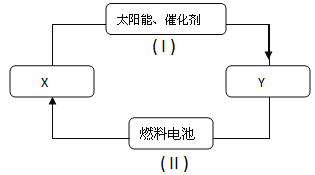
(1)从能量转换的角度看,过程II主要是将___能转化为____ 能。
(2)在该燃料电池中,H2所在的一极为_____极;若电解质溶液为碱性的KOH溶液,试写出两极的电极方程式:正极_______负极______________
【答案】 化学能 电能 负 O2+2H2O+4e-=4OH- H2-2e-+2OH-=2H2O
【解析】试题分析:本题考查化学反应中能量的转化,氢氧燃料电池电极反应式的书写。
(1)过程I是在太阳能、催化剂作用下将H2O分解成H2和O2,能量的转化将太阳能转化为化学能。过程II为燃料电池,燃料电池采用原电池原理,主要将化学能转化为电能。
(2)氢氧燃料电池的电池反应为2H2+O2=2H2O,H2发生失电子的氧化反应,H2所在一极为负极,若电解质溶液为碱性的KOH溶液,负极电极反应式为H2-2e-+2OH-=2H2O;O2发生得电子的还原反应,O2所在一极为正极,正极电极反应式为O2+2H2O+4e-=4OH-。

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目