题目内容
某可逆反应aA+bB?cC△H 在某温度下的平衡常数为K(K≠1),保持温度不变,将方程式的书写作如下改变,则△H和K数值的相应变化为( )A.写成2aA+2bB?2cC,△H、K值均扩大了一倍
B.写成2aA+2bB?2cC,△H扩大了一倍,K值保持不变
C.写成cC?aA+bB,△H、K值变为原来的相反数
D.写成cC?aA+bB,△H变为原来的相反数,K值变为倒数
【答案】分析:可逆反应aA+bB?cC△H,其K的表达式为生成物浓度幂之积与反应物浓度幂之积的比,△H的数值与化学计量数成正比,两个相反过程的△H的符号相反,数值相同,以此来解答.
解答:解:A.写成2aA+2bB?2cC,△H值均扩大了一倍,K的数值为原数值的平方倍,故A错误;
B.写成2aA+2bB?2cC,△H值均扩大了一倍,K的数值为原数值的平方倍,故B错误;
C.写成cC?aA+bB,△H变为原来的相反数,K值变为倒数,故C错误;
D.写成cC?aA+bB,△H变为原来的相反数,K值变为倒数,故D正确;
故选D.
点评:本题考查化学平衡常数的含义,注意在方程式不变的前提下,温度不变K不变,明确K的表达式及△H的数值与化学计量数的关系即可解答,题目难度中等.
解答:解:A.写成2aA+2bB?2cC,△H值均扩大了一倍,K的数值为原数值的平方倍,故A错误;
B.写成2aA+2bB?2cC,△H值均扩大了一倍,K的数值为原数值的平方倍,故B错误;
C.写成cC?aA+bB,△H变为原来的相反数,K值变为倒数,故C错误;
D.写成cC?aA+bB,△H变为原来的相反数,K值变为倒数,故D正确;
故选D.
点评:本题考查化学平衡常数的含义,注意在方程式不变的前提下,温度不变K不变,明确K的表达式及△H的数值与化学计量数的关系即可解答,题目难度中等.

练习册系列答案
相关题目
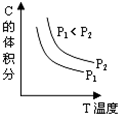 已知某可逆反应aA(g)+bB(g)?cC(g)+dD(g).反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的( )
已知某可逆反应aA(g)+bB(g)?cC(g)+dD(g).反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图.下列叙述正确的( ) cC
+ Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为(
)
cC
+ Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为(
)