题目内容
下列叙述中,正确的是
| A.用丁达尔现象实验可以区分食盐水和淀粉溶液 |
| B.氨气的水溶液能导电,所以氨气是电解质 |
| C.NO2、SO2溶于水都发生氧化还原反应 |
| D.Fe分别与氯气和稀盐酸反应可得到同一种氯化物 |
A
试题分析:A、食盐水属于溶液,淀粉溶液属于胶体,可用丁达尔现象实验鉴别,正确;B、氨气的水溶液能导电的原因是氨水中的NH3·H2O电离产生自由移动NH4+和OH-,NH3·H2O是电解质,NH3为非电解质,错误;C、NO2与水的反应为:3NO2+H2O=2HNO3+NO,属于氧化还原反应,SO2溶于水的反应为SO2+H2O=H2SO3,不是氧化还原反应,错误;D.Fe与氯气反应生成氯化铁,与稀盐酸反应生成氯化亚铁,错误。2、SO2和Fe的性质。

练习册系列答案
相关题目
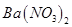 溶液可生成
溶液可生成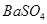 沉淀
沉淀