题目内容
8.下列物质可用于消毒杀菌的是( )①苯酚 ②硫磺 ③福尔马林 ④双氧水 ⑤次氯酸.
| A. | ①③⑤ | B. | ②④⑤ | C. | ①②④ | D. | 全部 |
分析 可用于消毒杀菌,则能是细菌的蛋白质变性,能使蛋白质变性的物质有强酸、强碱、强氧化性的物质、苯酚、硫磺、乙醇、丙酮、重金属盐等.
解答 解:可用于消毒杀菌,则能是细菌的蛋白质变性,能使蛋白质变性的物质有强酸、强碱、强氧化性的物质(如双氧水、次氯酸等)、苯酚、硫磺、乙醇、丙酮、重金属盐等.所以可用于消毒杀菌的物质有①苯酚 ②硫磺 ③福尔马林 ④双氧水 ⑤次氯酸.
故选D.
点评 本题考查了蛋白质的变性,题目难度不大,注意了解蛋白质变性的常用方法.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
18.等电子体具有相同的原子数目和电子数目,下列属于等电子体的是 ( )
| A. | NH3和H2O | B. | NO和O2+ | C. | NO2和CO2 | D. | OH-和NH2- |
19.[Co(NH3)4](H2O)2]3+具有几何异体构体的数目是( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
16.核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核有NMR现象.试判断下列哪组原子均可产生NMR现象( )
| A. | ${\;}_{\;}^{18}$O ${\;}_{\;}^{31}$P ${\;}_{\;}^{119}$Sn | |
| B. | ${\;}_{\;}^{27}$Al ${\;}_{\;}^{19}$F ${\;}_{\;}^{12}$C | |
| C. | 元素周期表中V A族所有元素的原子 | |
| D. | 元素周期表中第一周期所有元素的原子 |
20.某烃的结构简式为 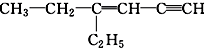 分子中饱和碳原子数为a,可能在同一直线上的碳原子数为b,可能在同一平面上的碳原子数最多为c,则a、b、c分别为( )
分子中饱和碳原子数为a,可能在同一直线上的碳原子数为b,可能在同一平面上的碳原子数最多为c,则a、b、c分别为( )
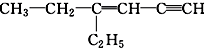 分子中饱和碳原子数为a,可能在同一直线上的碳原子数为b,可能在同一平面上的碳原子数最多为c,则a、b、c分别为( )
分子中饱和碳原子数为a,可能在同一直线上的碳原子数为b,可能在同一平面上的碳原子数最多为c,则a、b、c分别为( )| A. | 4、3、7 | B. | 4、3、8 | C. | 2、5、4 | D. | 4、6、4 |
17.铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.
Ⅰ、工业上一般以铁矿石、焦炭、石灰石和空气等为原料在高炉中炼制生铁
(1)高炉炼铁过程中加入石灰石的主要目的是将矿石中的二氧化硅等转变为炉渣.
(2)写出在高炉中铁矿石(以磁铁矿为例)被还原成单质铁的化学方程式Fe3O4+4CO$\frac{\underline{\;\;△\;\;}}{\;}$3Fe+4CO2.
Ⅱ、碱式硫酸铁[Fe(OH)SO4]是一种用语污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁)生产碱式硫酸铁的工艺流程如下:
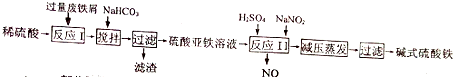
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(3)写出反应Ⅰ中发生的置换反应的离子方程式Fe+2H+═Fe2++H2↑.
(4)加入少量NaHCO3的目的是调节溶液的pH,应控制pH的范围区间为[4.4~7.5).
(5)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若通入2.8LO2(标准状况),则相当于节约NaNO2的质量为34.5g.
(6)碱式硫酸铁溶于水后产生的[Fe(OH)]2+离子,可部分水解生成[Fe(OH)SO4]2-聚合离子,该水解反应的离子方程式为2[Fe(OH)]2++2H2O═[Fe2(OH)4]2++2H+.
Ⅲ、铁的化合物也是制备高能锂电池的重要材料,已知LiFePO4电池反应为FePO4+Li$\frac{放电}{充电}$LiFePO4,电池中的固体电解质可传到Li+写出该电池充电时阳极反应式LiFePO4-e-═FePO4+Li+,常温下以该电池为电源电解500mL饱和食盐水,当消耗0.35gLi时,溶液的pH值为13(忽略溶液的体积变化).
Ⅰ、工业上一般以铁矿石、焦炭、石灰石和空气等为原料在高炉中炼制生铁
(1)高炉炼铁过程中加入石灰石的主要目的是将矿石中的二氧化硅等转变为炉渣.
(2)写出在高炉中铁矿石(以磁铁矿为例)被还原成单质铁的化学方程式Fe3O4+4CO$\frac{\underline{\;\;△\;\;}}{\;}$3Fe+4CO2.
Ⅱ、碱式硫酸铁[Fe(OH)SO4]是一种用语污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁)生产碱式硫酸铁的工艺流程如下:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(4)加入少量NaHCO3的目的是调节溶液的pH,应控制pH的范围区间为[4.4~7.5).
(5)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若通入2.8LO2(标准状况),则相当于节约NaNO2的质量为34.5g.
(6)碱式硫酸铁溶于水后产生的[Fe(OH)]2+离子,可部分水解生成[Fe(OH)SO4]2-聚合离子,该水解反应的离子方程式为2[Fe(OH)]2++2H2O═[Fe2(OH)4]2++2H+.
Ⅲ、铁的化合物也是制备高能锂电池的重要材料,已知LiFePO4电池反应为FePO4+Li$\frac{放电}{充电}$LiFePO4,电池中的固体电解质可传到Li+写出该电池充电时阳极反应式LiFePO4-e-═FePO4+Li+,常温下以该电池为电源电解500mL饱和食盐水,当消耗0.35gLi时,溶液的pH值为13(忽略溶液的体积变化).
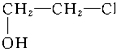 ②
②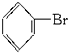 ③CH2Cl2 ④CCl4.
③CH2Cl2 ④CCl4.