题目内容
氨是最重要的氮肥,是产量最大的化工产品之一。中学化学课本里学到的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的。他因此获得了1918年度诺贝尔化学奖。哈伯法合成氨需要20~50MPa的高压和500℃的高温,并用铁作催化剂。近一个世纪来,全世界都这样生产氨。合成氨需要高温高压,似乎是天经地义了。然而,2001年有两位希腊化学家在《科学》杂志上发表文章,在常压下把氢气和用氦稀释的氮气分别通入一个加热到570℃的电解池(见图),氢气和氮气在电极上合成了氨,而且转化率达到了78%!,对比哈伯法合成氨转化率仅10%~15%,听起来真像天方夜谭。请根据以上的材料回答下列问题:
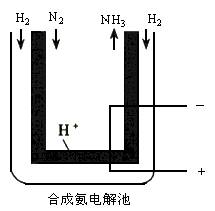
(1)新法合成氨的电解池中能否用水溶液作电解质?为什么?
(2)新法合成氨中所用的电解质(图中涂色处)能传导H+,试写出电极反应和总反应式。
解析:
精析 题中新信息较多,这里第一步是抓住关键信息。看完题目,每个解题者都会注意到新法合成氨的反应条件是“常压、570℃”,反应物是“氢气、氮气”,反应装置是“电解池”。由此入手,就可用类比与联想的方法解答本题。①从“常压、570℃”入手,联想到水在常压下的沸点只有100℃。所以不能用水溶液作电解质。(实际上是用某种“固体电解质”,2000年高考理科综合能力测试卷中曾出现了“固体电解质”)。②反应物是氢气、氮气,产物当然是氨,所以总反应式即电解池的总反应式为: 3H2+N2 与已学过的电解反应进行类比,可得出氢气通入电解池的阳极,氮气应通入电解池的阴极。从题示新信息还可得到,所用电解池中的电解质能传导H+,所以书写电极反应式时可以用H+配平。综合以上几点可写出电极反应式:阳极:3H2-6e-=6H+(生成的H+通过电解质传导到阴极)。阴极:N2+6H++6e-=2NH3。 答案(1)不能,因为水在常压下的沸点只有100℃ (2)阳极:3H2-6e-=6H+ 阴极:N2+6H++6e-=2NH3 3H2+N2
|


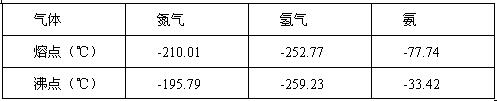
反应体系中各组分的部分性质见下表:
气体 | 氮气 | 氢气 | 氨 |
熔点/℃ | -210.01 | -252.77 | -77.74 |
沸点/℃ | -195.79 | -259.23 | -33.42 |
(1)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程,即反应后通过把混合气体的温度降低到____________,使混合气体分离出产品,N2、H2继续循环。写出该反应的化学平衡常数表达式:K=____________。
(2)运用化学反应速率和化学平衡的观点说明工业上采用“使混合气体分离出产品,N2、H2继续循环”的生产措施的理由:___________________________________________________。
(3)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为_____________________________。
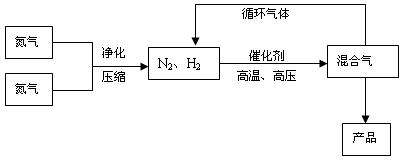
(4)合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g) ![]() 2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如下图甲所示。下列叙述正确的是____________。
2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如下图甲所示。下列叙述正确的是____________。
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773 K下反应至t1时刻,n(H2)比图中d点的值大
(5)1998年希腊亚里斯多德大学的Marncellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨,其实验装置如下图乙。阴极的电极反应式为__________________________________________________________________。


甲 乙
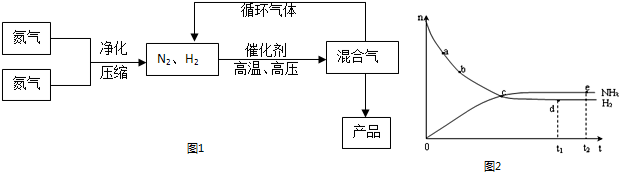
(15分)氨是最重要的氮肥,是产量最大的化工产品之一。课本里介绍的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的,其合成原理为:N2(g)+3H2(g)  2NH3(g);△H<0他因此获得了1918年诺贝尔化学奖。工业上合成氨的部分工艺流程如下:
2NH3(g);△H<0他因此获得了1918年诺贝尔化学奖。工业上合成氨的部分工艺流程如下:

|
气体 |
氮气 |
氢气 |
氨 |
|
熔点(℃) |
-210.01 |
-252.77 |
-77.74 |
|
沸点(℃) |
-195.79 |
-259.23 |
-33.42 |
反应体系中各组分的部分性质见上表:
(1)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到 ℃使混合气体分离出来产品;继续循环的气体是 。
(2)工业上采取用上述(1)操作的目的:
。
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________ 。
(4)合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应: N2(g)+3H2(g) 2NH3(g),在673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g),在673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是

A.点a的正反应速率比点b的大
B.点 c处反应达到平衡
C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻, n(H2)比上图中d点的值大