题目内容
已知氮的氧化物具有氧化性,能与灼热的铜反应生成氧化铜和氮气.现将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,生成的气体体积为11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为( )
| A、NO2 | B、N2O5 | C、N2O | D、N2O4 |
分析:氮氧化合物气体的物质的量为1mol,生成气体的物质的量为0.5mol,应为氮气,根据氮原子质量守恒可知应为NO2.
解答:解:氮氧化合物气体的物质的量为1mol,生成气体的物质的量为0.5mol,应为氮气,假设反应为:2NxOy+2yCu
2yCuO+xN2,
根据氮原子守恒可知x=1,应为NO2,即发生4Cu+2NO2=4CuO+N2.
故选A.
| ||
根据氮原子守恒可知x=1,应为NO2,即发生4Cu+2NO2=4CuO+N2.
故选A.
点评:本题考查氮氧化物的知识,题目难度不大,侧重于阿伏伽德罗定律的考查,可运用质量守恒定律解答该题.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案
相关题目
 L B.
L B. L C.
L C. L D.
L D. L
L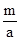 L B.
L B. 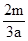 L
C.
L
C. 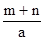 L
D.
L
D. 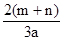 L
L