��Ŀ����
17��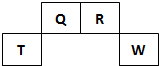 ������Ԫ��Q��R��T��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������T��������������������������ȣ���ش��������⣺
������Ԫ��Q��R��T��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������T��������������������������ȣ���ش��������⣺��1��T�����ӽṹʾ��ͼΪ
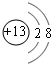 ��
����2��Ԫ�صķǽ����ԣ�Q����R���ǿ�ڡ������ڡ�����
��3����Qͬ����Ķ�����Ԫ���γɵ�����������ԭ�Ӿ��壨������ͣ���
��4��д��W���⻯��ĵ���ʽ
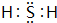 ��ԭ��������W��1��Ԫ���䵥����ʹW���⻯��ˮ��Һ����ǣ�д����Ӧ�Ļ�ѧ����ʽCl2+H2S=S��+2HCl��
��ԭ��������W��1��Ԫ���䵥����ʹW���⻯��ˮ��Һ����ǣ�д����Ӧ�Ļ�ѧ����ʽCl2+H2S=S��+2HCl����5��R�ж�����������м���Է���������С����һ�������£�2L�ļ�������0.5L���������ϣ����û�����屻������NaOH��Һ��ȫ���պ�û����������������ɵ�R�ĺ������εĻ�ѧʽ��NaNO2��
���� �ɶ�����Ԫ��Q��R��T��W������λ�ã���ȷ��T��WΪ�������ڵ�Ԫ�أ�Q��RΪ�ڶ�����Ԫ�أ�T������������������������ȣ���TΪAlԪ�أ���QΪCԪ�أ�RΪNԪ�أ�WΪSԪ�أ�
��1��T������ΪAl3+�����Ӻ�����2�����Ӳ㣬���������Ϊ2��8��
��2��ͬ�����������Ԫ�طǽ�������ǿ
��3����Qͬ����Ķ�����Ԫ��ΪSi���γɵ�������ΪSiO2������ԭ�Ӿ��壻
��4��W���⻯��ΪH2S����������ԭ������ԭ��֮���γ�1�Թ��õ��Ӷԣ�ԭ��������W��1��Ԫ��ΪCl������������ˮ��Һ��Ӧ����S��HCl��
��5��RΪNԪ�أ��ж�����������м���Է���������С�����ΪNO�����ݵ���ת���غ��������������NԪ�ػ��ϼۣ�����ȷ�������ɵ�R�ĺ������εĻ�ѧʽ��
��� �⣺�ɶ�����Ԫ��Q��R��T��W������λ�ã���ȷ��T��WΪ�������ڵ�Ԫ�أ�Q��RΪ�ڶ�����Ԫ�أ�T������������������������ȣ���TΪAlԪ�أ���QΪCԪ�أ�RΪNԪ�أ�WΪSԪ�أ�
��1��T������ΪAl3+�����ӽṹʾ��ͼΪ  ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��ͬ�����������Ԫ�طǽ�������ǿ���ʷǽ�����Q��R���ʴ�Ϊ�����ڣ�
��3����Qͬ����Ķ�����Ԫ��ΪSi���γɵ�������ΪSiO2������ԭ�Ӿ��壬�ʴ�Ϊ��ԭ�Ӿ��壻
��4��W���⻯��ΪH2S������ʽΪ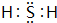 ��ԭ��������W��1��Ԫ��ΪCl���䵥����ʹW���⻯��ˮ��Һ����ǣ��÷�Ӧ�Ļ�ѧ����ʽΪ��Cl2+H2S=S��+2HCl��
��ԭ��������W��1��Ԫ��ΪCl���䵥����ʹW���⻯��ˮ��Һ����ǣ��÷�Ӧ�Ļ�ѧ����ʽΪ��Cl2+H2S=S��+2HCl��
�ʴ�Ϊ��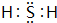 ��Cl2+H2S=S��+2HCl��
��Cl2+H2S=S��+2HCl��
��5��RΪNԪ�أ��ж�����������м���Է���������С�����ΪNO����һ�������£�2L�ļ�������0.5L���������ϣ����û�����屻������NaOH��Һ��ȫ���պ�û�����������������������NԪ�ػ��ϼ�Ϊa�����ݵ���ת���غ㣺2��a-2��=0.5��4�����a=3�������ɵ�R�ĺ������εĻ�ѧʽ��NaNO2��
�ʴ�Ϊ��NaNO2��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ���ּ�ڿ���ѧ���Ի���֪ʶ�Ĺ��̣�

 ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д� ����������ϵ�д�
����������ϵ�д�| A�� | ����Һ����1Lˮ���ܽ�0.1molBa��NO3��2�Ƶ� | |
| B�� | 1L��Һ�к���Ba2+��NO3-��������Ϊ3NA | |
| C�� | 0.5L��Һ��Ba2+���ӵ����ʵ���Ũ��Ϊ0.2 mol•L-1 | |
| D�� | 0.5L��Һ��NO3-���ӵ����ʵ���Ũ��Ϊ0.2 mol•L-1 |
| A�� | ��ͬ�����HA��HB��Һ��HA��Һ�ĵ�����ǿ��˵������HA��HB | |
| B�� | �Ȼ�������ˮ���ڵ���������������Na+��Cl- | |
| C�� | NaOH��Һ��ˮϡ�ͣ���Һ����������Ũ�Ⱦ���С | |
| D�� | �ᡢ��Ρ�ijЩ���������ˮ���ǵ���� |
| �¶�/�� | 10 | 20 | 30 | 40 | 50 |
| KCl | 30g | 33g | 35g | 38g | 41g |
| KNO3 | 21g | 31g | 45g | 65g | 88g |
| A�� | KNO3��KCl���ܽ�ȴ� | |
| B�� | �������ʵ��ܽ����ȵ��¶���20��30��� | |
| C�� | ��20��ʱ��10gˮ�м���5gKCl�ɵõ�33.3% ��KCl��Һ | |
| D�� | ��50��ʱ�������ʸ�5g�ֱ����l0gˮ�У�����ܽ⣬���й���ʣ�� |
| A�� | Cl- | B�� | Cl2 | C�� | H+ | D�� | Cu2+ |
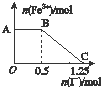
| A�� | ����ʽ�е�XΪ2MnSO4 | |
| B�� | �����ԣ�KMnO4��Fe3+��I2 | |
| C�� | ����OC�ε����ݿ�֪��ʼ����ĸ�����ص����ʵ���Ϊ0.30 mol | |
| D�� | AB���Ǹ�����غ͵⻯����Һ��Ӧ��BC�εķ�ӦΪ2Fe3++2I-�T2Fe2++I2 |
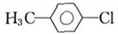
 ��һ�ֳ����Ļ�ױƷ��ù������������������ͼ����Ӧ����û��ȫ��ע������
��һ�ֳ����Ļ�ױƷ��ù������������������ͼ����Ӧ����û��ȫ��ע������
 ��
�� ��
��
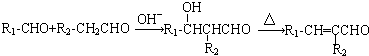
 ����Ӧ�١���������ȡ����Ӧ���Тۢܢݣ�����ţ���
����Ӧ�١���������ȡ����Ӧ���Тۢܢݣ�����ţ���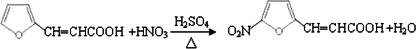 ��
�� ��
��