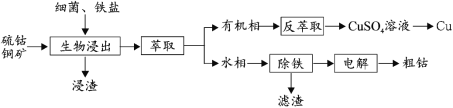
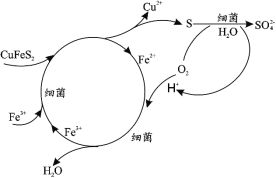
��Ŀ����
����Ŀ��SO2�ǿ�������Ҫ�Ĵ�����Ⱦ����ҹ涨���ŷ�ǰ���뾭��������
��Һ���շ�����ҵ�ϳ���NaOH��Һ������Һ��
��1����0.5L1 mol��L��1��NaOH��Һ��ͨ���״̬��11.2L��SO2��
��д����Ӧ�����ӷ���ʽ__________��
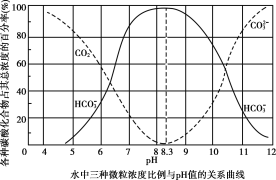
����֪��Ka1��1.54��10��2��Ka2��1.02��10��7����������Һ��_______������ԡ��������ԡ������ԡ����������й�����Һ������Ũ�ȴ�С��ϵ��ȷ����_________��
A c��H2SO3����c��SO32����
B c��Na������c��H+����c��HSO3������2c��SO32������c��OH����
C c��Na������c��H2SO3����c��HSO3������c��SO32����
D c��Na������c��HSO3������c��SO32������c��H+����c��OH����
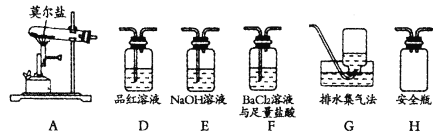
��2����ҵ��Ҳ������Na2SO3��Һ����SO2�����õ�ⷨ��������SO2��������Һ��ʵ������Һ�Ļ��������ã�װ������ͼ��ʾ��
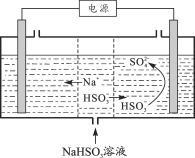
�ٹ���һ��ʱ�����������Һ��pH_______�����������С�����䡱����
��д�������ĵ缫��Ӧʽ_______��
��SO2�Ļ������ã�
��3��SO2��Cl2��Ӧ���Ƶû����ȣ�SO2Cl2������ӦΪSO2��g����Cl2��g��![]() SO2Cl2��g������Ͷ�ϱ�1:1��SO2��Cl2����һ��ѹ���ܱ������з���������Ӧ��SO2��ת�������¶�T�Ĺ�ϵ����ͼ��ʾ��
SO2Cl2��g������Ͷ�ϱ�1:1��SO2��Cl2����һ��ѹ���ܱ������з���������Ӧ��SO2��ת�������¶�T�Ĺ�ϵ����ͼ��ʾ��
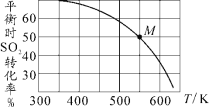
�� �÷�Ӧ����H________���������������������0��
�� ����Ӧһֱ������pѹǿ�����½��У���M��ķ�ѹƽ�ⳣ��Kp��_____���ú�p�ı���ʽ��ʾ����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�������������
���𰸡�2OH����SO2=HSO3�� ���� BC ���� HSO3����2e����2H2O=3H+��SO42�� �� 3/p
��������
��(1)�����ж�����NaHSO3���ٸ����غ�����жϹ�ϵ��
(2)������������Һ�е������ӷŵ磻
����װ��ͼ��֪���ұ�Ϊ���������ʧ�����ױ�����Ϊ�������Ϊ������
��(3)�ٽ���¶ȶԷ�Ӧ���ʵ�Ӱ��ش�
�ڸ�������ʽ��⡣
��(1) �ٱ�״����11.2L��SO2�����ʵ���Ϊ![]() =0.5mol��0.5L1 mol��L��1��NaOH�����ʵ���Ϊ
=0.5mol��0.5L1 mol��L��1��NaOH�����ʵ���Ϊ![]() =0.5mol����1��1��Ӧ������NaHSO3�������ӷ���ʽΪ2OH����SO2=HSO3�����ʴ�Ϊ2OH����SO2=HSO3����
=0.5mol����1��1��Ӧ������NaHSO3�������ӷ���ʽΪ2OH����SO2=HSO3�����ʴ�Ϊ2OH����SO2=HSO3����
����֪��Ka1��1.54��10��2��Ka2��1.02��10��7����֪HSO3���ĵ������ˮ�⣬��Һ�����ԣ�
A. HSO3���ĵ������ˮ��, �� c��H2SO3����c��SO32������A�����
B.���ݵ���غ㣺 c��Na������c��H+����c��HSO3������2c��SO32������c��OH������B����ȷ��
C.����Ԫ���غ㣺 c��Na������c��H2SO3����c��HSO3������c��SO32������C����ȷ��
D. HSO3���ĵ������ˮ�⣬��ˮ����������ӣ�����ȷ������Ϊc��Na������c��HSO3������c��H+����c��SO32������c��OH������D����ʴ�ΪBC��
(2)�ٵ����У�����������Һ�е������ӷŵ磬�缫��ӦʽΪ��2H++2e-=H2������pH���ʴ�Ϊ������
����װ��ͼ��֪���ұ�Ϊ���������ʧ�����ױ�����Ϊ�������Ϊ��������缫��ӦʽΪHSO3--2e-+2H2O��SO42-+3H+���ʴ�Ϊ��HSO3����2e����2H2O=3H+��SO42��
��3���ٸ���ͼ�������¶ȣ�SO2��ת���ʼ�С��˵��ƽ�������ƶ���˵���÷�Ӧ����ӦΪ���ȷ�Ӧ����H��0���ʴ�Ϊ����
����SO2�����ʵ���Ϊ1mol����Cl2�����ʵ���Ϊ1mol��������ʽ���£�
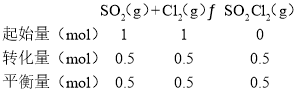
ƽ�ⳣ��K=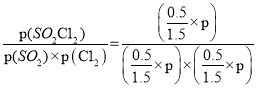
![]() =
=![]() ���ʴ�Ϊ��3/p��
���ʴ�Ϊ��3/p��

����Ŀ��ij�о���ѧϰС������H2C2O4��Һ������KMnO4��Һ�ķ�Ӧ̽������������ĸı�Ի�ѧ��Ӧ���ʵ�Ӱ����������������ʵ�飺
ʵ����� | ʵ�� �¶�/K | �й����� | ��Һ��ɫ������ɫ����ʱ��/s | ||||
����KMnO4��Һ | H2C2O4��Һ | H2O | |||||
V/mL | c/mol��L-1 | V/mL | c/mol��L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
��1��ͨ��ʵ��A��B����̽����___(���ⲿ����)�ĸı�Ի�ѧ��Ӧ���ʵ�Ӱ�죬����V1��____��T1��____��ͨ��ʵ��___(��ʵ�����)��̽�����¶ȱ仯�Ի�ѧ��Ӧ���ʵ�Ӱ�죬����V2��____��
��2����t1��8�����ɴ�ʵ����Եó��Ľ�����_____��������Һ����ı仯������ʵ��B�����ݼ��㣬0��8s�ڣ���KMnO4��Ũ�ȱ仯��ʾ�ķ�Ӧ����v(KMnO4)��___��
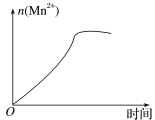
��3����С���һλͬѧͨ���������Ϸ��֣�����ʵ�������n(Mn2+)��ʱ��ı仯�����ͼ��ʾ������Ϊ������ֱ仯��ԭ���Ƿ�Ӧ��ϵ�е�ij�����Ӷ�KMnO4�����֮��ķ�Ӧ��ij���������ã����������____����Ӧ�������������___(�����ӷ���)��