题目内容
等体积浓度均为0.1mol/L的三种溶液:①CH3COOH溶液、②HSCN溶液、③NaHCO3溶液混合,①、②分别与③混合,实验测得产生的CO2气体体积(V)随时间(t)的变化如图所示,下列说法正确的是( )

A. 三种溶液pH的比较③>②>①
B. 反应结束后所得两溶液中,c(CH3COO-)>c(SCN-)
C. 上述三种溶液中水电离的电离度:NaHCO3>CH3COOH>HSCN
D. ①与③反应所得的溶液中:c(CH3COO-) + c(CH3COOH) = 0.1mol/L
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:
CO(g)+Cl2(g) COCl2(g)
COCl2(g)
其中容器Ⅰ中5 min时到达平衡。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法正确的是
A. 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B. 该反应的正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D. 若起始时向容器Ⅰ中加入CO 0.8 mol、Cl2 0.8 mol,达到平衡时CO的转化率大于80%


 CaCO3(s)+SO42-的平衡常数K=1.75×104,已知常温下,饱和CaSO4溶液中c( Ca2+) = 0.70×10-2mol/L,则常温时CaCO3的Ksp为
CaCO3(s)+SO42-的平衡常数K=1.75×104,已知常温下,饱和CaSO4溶液中c( Ca2+) = 0.70×10-2mol/L,则常温时CaCO3的Ksp为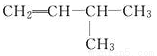 2-甲基-3-丁烯
2-甲基-3-丁烯 CCH3 2-丁炔
CCH3 2-丁炔 1,5-二甲苯
1,5-二甲苯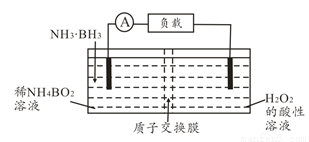
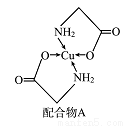

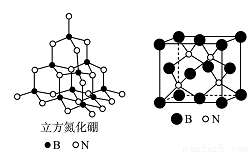
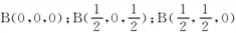 等。则距离上述三个B原子最近且等距的N原子的坐标参数为____________________ 。
等。则距离上述三个B原子最近且等距的N原子的坐标参数为____________________ 。 2N2(g)+CO2(g)+2H2O(g) ΔH=QkJ·mol-1,写出上述反应的平衡常数表达式_______,已知该反应的平衡常数K随温度升高而减小,则Q_______0(填“>”或“<”或“=”)。
2N2(g)+CO2(g)+2H2O(g) ΔH=QkJ·mol-1,写出上述反应的平衡常数表达式_______,已知该反应的平衡常数K随温度升高而减小,则Q_______0(填“>”或“<”或“=”)。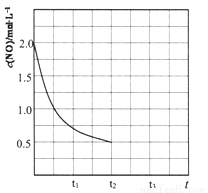

 CH3OH(g)。该反应的△H=-91.kJ·mol-1
CH3OH(g)。该反应的△H=-91.kJ·mol-1